 |
Главная |
Лабораторная работа 27-28
|
из
5.00
|
Тема: Выполнение расчетов в объемном анализе
Цель:
Обучающая– формирование умений проведения вычислений в объемном анализе
Развивающая – глубокое изучение различных явлений и законов по данной теме ;
Воспитательная – приобщать обучающихся к активности, самостоятельности на лабораторных занятиях
Форма урока:практическая работа
Ход урока:
1. Объяснение типовой задачи - 20 минут
2.Решение задачи у доски - 25 минут
3.Самостоятельное решение - 50 минут
I. Какую массу навески фосфорной кислоты H3PO4 необходимо взять для приготовления 2 л 0,06 н. раствора H3PO4?
Дано: Решение:
V H3PO4 = 2 л 1. Вычислим молярную массу (М H3PO4= Мr H3PO4) и
C H3PO4 = 0,06 н. эквивалентную массу H3PO4 (Мэ H3PO4):
m H3PO4 = ? Мr H3PO4 = 1∙3 + 31 + 16∙4 = 98 (г/моль)
Мэ H3PO4 = Мr H3PO4/3 = 98/3 = 32,7 (г/моль)
2. Вычислим количество вещества эквивалентов H3PO4, содержащееся в 2 л раствора?
В 1 л раствора – 0,06 моль экв. H3PO4
В 2 л раствора – х моль экв. H3PO4
2 ∙ 0,06
х = ----------- = 0,12 (моль)
1 В 2 л 0,06 н. раствора содержится 0,12 моль H3PO4
3. Вычислим массу навески H3PO4:
1 моль эквивалентов H3PO4 составляет 32, 7 г
0,12 моль эквивалентов H3PO4 - х г
0,12 ∙ 32,7
х = ------------- = 3,92 (г) 1
Массу навески также можно рассчитать по формуле:
c ∙ Мэ ∙ V
m = ------------
Ответ: масса навески H3PO4 равна 3,92 г.
II. В 250 мл раствора содержится 6 г карбоната калия K2CO3. Вычислите нормальную концентрацию раствора K2CO3.
| Дано: V K2CO3 = 250 мл m K2CO3 = 6 г c( K2CO3) = ? | Решение:
1. Вычислим молярную массу (М K2CO3= Мr K2CO3) и эквивалентную массу K2CO3 (Мэ K2CO3):
Мr K2CO3 = 39∙2 + 12 + 16∙3 = 138(г/моль)
Мэ K2CO3 = Мr K2CO3/2 = 138/2 = 69 (г/моль)
2. Вычислим массу K2CO3, содержащуюся в 1 л раствора:
В 250 мл содержится 6 г K2CO3
В 1000 мл – х г K2CO3
1000 ∙ 6
х = ---------- = 24 (г)
В 1000 мл раствора содержится 24 г K2CO3
3. Вычислим нормальную концентрацию раствора K2CO3:
1 моль эквивалентов K2CO3 составляет 69 г
х моль эквивалентов K2CO3 составляет 24 г
х = 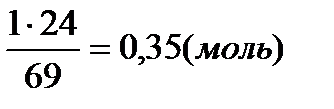 в 1 л раствора содержится 0,35 моль эквивалентов K2CO3. Нормальную концентрацию раствора можно, также вычислить по формуле, приведенной в примере I.
Ответ: N(K2CO3) = 0,35 моль
в 1 л раствора содержится 0,35 моль эквивалентов K2CO3. Нормальную концентрацию раствора можно, также вычислить по формуле, приведенной в примере I.
Ответ: N(K2CO3) = 0,35 моль
|
III. Вычислите титр раствора, если в 25,00 мл содержится 0,5 г NaOH.
Дано: Решение:
V(NaOH)= 25,00 мл Титр раствора находим по формуле:
m (NaOH) = 0,5 г m 0,5
T = ------ = ------- = 0,02 (г/мл)
T NaOH = ? V 25,00
Ответ: Т NaOH = 0,02 г/мл
IV. Вычислите нормальную концентрацию раствора H2SO4, если на нейтрализацию 24,50 мл его израсходовано 23,00 мл 0,15 н.раствора КОН.
Дано: Решение:
V (H2SO4) = 24,50 мл 1. Составим уравнение реакции нейтрализации:
V КОН = 23,00 мл H2SO4 + 2 КОН = К2SO4 + 2 H2O
N КОН = 0,15 н.
2. Вычислим нормальную концентрацию H2SO4:
С ( H2SO4) = ? на основании закона эквивалентов:
C ( КОН) ∙ V (КОН) 0,15 ∙ 23,00
C (H2SO4) = -------------------- = --------------- = 0, 14 (моль/л)
V (H2SO4) 24,50
Ответ: C(H2SO4) = 0, 14 моль/л
V. Навеска Ba(OH)2 растворена в мерной колбе на 250,00 мл. Объем раствора доведен до метки. На титрование 25,00 мл полученного раствора израсходовано 23,00 мл 0,09908 н. раствора HCl. Вычислите, сколько граммов Ba(OH)2 содержится в навеске.
Дано: Решение:
V р-ра = 250,00 мл 1. Составим уравнение реакции нейтрализации:
V Ba(OH)2 = 25,00 мл Ba(OH)2 + 2HCl = BaCl2 + 2Н2О
V HCl = 23,00 мл 2. Вычислим нормальную концентрацию раствора
N HCl = 0,09908 н. Ba(OH)2, используя закон эквивалентов:
m (HCl)= ? C HCl ∙ V HCl 0,09908 ∙ 23,00
C Ba(OH)2= -------------------- = --------------- = 0,091 (моль/л)
V Ba(OH)2 25,00
1. Вычислим молярную массу (М Ba(OH)2= Мr Ba(OH)2) и эквивалентную массу Ba(OH)2 (Мэ Ba(OH)2):
Мr Ba(OH)2 = 137 + (16 + 1) ∙ 2 = 171 (г/моль)
Мэ Ba(OH)2 = Мr Ba(OH)2 /2 = 171/2 = 85,5 (г/моль)
4. Вычислим навеску Ba(OH)2 по формуле:
C ∙ Мэ ∙ V 0,091∙85,5∙250,00
m(HCl) = ------------ = ----------------------- = 1,95 (г)
1000 1000
Ответ: m(HCl) = 1,95 г
VI. На титрование 0,2650 г щавелевой кислоты H2C2O4 ∙ 2 H2O, растворенной в произвольном объеме воды, израсходовано 49,20 мл раствора щелочи NaOH. Определите нормальную концентрацию и титр раствора NaOH.
Дано: Решение:
m H2C2O4 ∙ 2 H2O = 0,2650 г 1. Составим уравнение реакции полной
V NaOH=49,20 мл нейтрализации:
2 NaOH + H2C2O4 = Na2C2O4 + 4 H2O
C NaOH = ? 2 моль 1 моль
Т NaOH = ?
2. Вычислим молярную массу (М NaOH =Мr NaOH),
молярную массу (М H2C2O4 ∙ 2 H2O =Мr H2C2O4 ∙ 2 H2O) и эквивалентную массу NaОН (Мэ NaOH):
Мr NaOH = 23 + 16 + 1 = 40 (г/моль)
Мr H2C2O4 ∙ 2 H2O = 1∙2+12∙2+16∙4+2 (1∙2+16) = 126 (г/моль)
Мэ NaOH = Мr NaOH /1 = 40 (г/моль)
3. Вычислим массу NaOH содержащуюся в 49,20 мл раствора:
По уравнению реакции масса 1 моль H2C2O4 ∙ 2 H2O эквивалентна массе 2 моль NaOH, а навеска 0,2650 г H2C2O4 ∙ 2 H2O эквивалентна массе NaOH , содержащегося в 49,20 мл раствора NaOH. Составим пропорцию:
2 ∙ 40 г NaOH соответствует 126 г H2C2O4 ∙ 2 H2O
х г NaOH ----- 0,2650 г H2C2O4 ∙ 2 H2O
2 ∙ 40 ∙ 0,2650
х = ------------------ = 0,17 (г)
В 49,20 мл раствора NaOH содержится 0,17 г.
2. Вычислим титр раствора NaOH:
g 0,17
Т =---- = -------- = 0,0034 (г/мл)
V 49,20
3. Вычислим нормальную концентрацию раствора NaOH, используя формулу: Т ∙ 1000 0,0034 ∙ 1000
N = ---------- = ---------------- = 0,085 (моль/л)
Мэ 40
Ответ: N NaOH = 0,085 моль/л;
Т NaOH = 0,0034 г/мл
VII. Вычислите Т HCl по NaOH, если нормальная концентрация раствора HCl равна 0,1105 н.
Дано: Решение:
C HCl = 0,1105 н. 1. Составим уравнение реакции полной нейтрализации:
NaOH + HCl = NaCl + H2О
Т HCl/NaOH = ? 1 моль 1 моль
2. Вычислим молярную массу (М NaOH = Мr NaOH)
и эквивалентную массу NaОН (Мэ NaOH):
Мr NaOH = 23 + 16 + 1 = 40 (г/моль)
Мэ NaOH = Мr NaOH /1 = 40 (г/моль)
- Выражение Т HCl/NaOH показывает, сколько граммов NaOH соответствует 1 мл раствора HCl данной концентрации. Раствор HCl содержит в 1000 мл 0,1105 моль эквивалентов соляной кислоты. Следовательно, в 1 мл НСl содержится 0,1105/1000 моль эквивалентов HCl, которое взаимодействует с таким же количеством моль эквивалентов NaOH.
- Приведем формулу расчета:
N HCl ∙ Мэ NaOH 0,1105 ∙ 40
Т HCl/NaOH = ----------------------- = -------------- = 0,00442 (г/мл)
1000 1000
Ответ: Т HCl/NaOH = 0,00442 г/мл
|
из
5.00
|
Обсуждение в статье: Лабораторная работа 27-28 |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

