 |
Главная |
Методы получение простых эфиров
|
из
5.00
|
Простые эфиры – органические вещества, имеющие формулу R-O-R1 где R и R1 – углеводородные радикалы.
Симметричные простые эфиры R–O–R получают при межмолекулярной дегидратации спиртов.
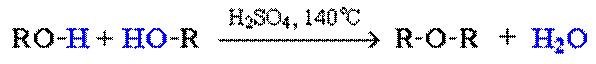
Эфиры несимметричного строения R–O–R1 образуются при взаимодействии алкоголята и галогенуглеводорода (синтез Вильямсона). Например, метилэтиловый эфир можно получить из этилата натрия и хлорметана:
C2H5ONa + CH3Cl  C2H5OCH3 + NaCl
C2H5OCH3 + NaCl
Понятие о восстанавливающих и невосстанавливающих углеводах.
Группы восстанавливающих (невосстанавливающих) углеводов есть в составе дисахаридов. Например, в составе мальтозы у второго остатка моносахарида (глюкозы) имеется свободный полуацетальный гидроксил, придающий данному дисахариду восстанавливающие свойства.
 Мальтоза
Мальтоза
Если в составе дисахарида нет данного полуацетального гидроксила, то дисахарид относят к невосстанавливающим.
Изомеры алкана
Алкан С4Н10 – бутан. Изомеры: 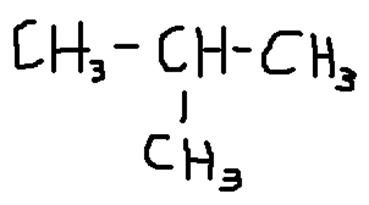
- 2-метилпропан (изобутан)

- циклобутан
Пропин
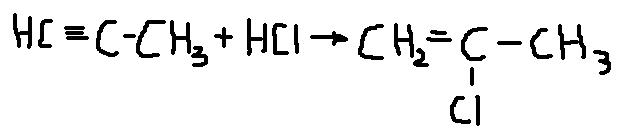
- 2- хлорпропен
Понятие ВМС( мономер, элементарное звено, степень полимеризации, полимер) на примере полипропилена.
Пропилен СН2=СH–CH3 является мономером полипропилена:
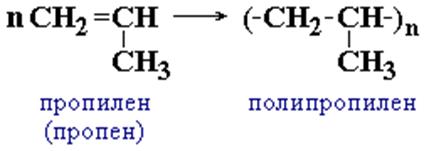
элементарное звено: 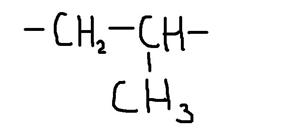 ,
,
степень полимеризации n раз (где n = 100 – 1000), полимер в данном случае будет выглядеть следующим образом
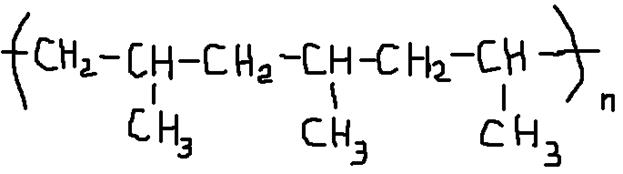
19. Химические свойства алканов:
Галогенирование— это одна из реакций замещения. Галогенирование алканов проходит поэтапно — за один этап замещается не более одного атома водорода:
1. CH4 + Cl2 → CH3Cl (хлорметан) + HCl
2. CH3Cl + Cl2 → CH2Cl2 (дихлорметан
) + HCl3. CH2Cl2 + Cl2 → CHCl3 (трихлорметан) + HCl
4. CHCl3 + Cl2 → CCl4 (тетрахлорметан) + HCl.
Нитрование:
Алканы реагируют с 10 % раствором азотной кислоты или оксидом азота NO2 в газовой фазе при температуре 140 °C и небольшом давлении с образованием нитропроизводных.
RH + HNO3 → RNO2 + H2O.
Горение
Основным химическим свойством предельных углеводородов, определяющих их использование в качестве топлива, является реакция горения. Пример:
CH4 + 2O2 → CO2 + 2H2O + Q.
Каталитическое окисление
Могут образовываться спирты, альдегиды, карбоновые кислоты.
Разложение
Реакции разложения происходят лишь под влиянием больших температур. Повышение температуры приводит к разрыву углеродной связи и образованию свободных радикалов.
CH4 → C + 2H2 (t > 1000 °C).
Изомеризация:
Под действием катализатора (например, AlCl3) происходит изомеризация алкана: например, бутан (C4H10), взаимодействуя с хлоридом алюминия (AlCl3), превращается из н-бутана в 2-метилпропан.
Алифатические амины. Их классификация Амины – органические соединения, являющиеся производными аммиака, в молекуле которого одни, два или три атома водорода замещены на углеводородные радикалы.
По числу замещённых атомов водорода различают соответственно первичные, вторичные и третичные амины. Четвертичное аммониевое соединение вида [R4N]+Cl- является органическим аналогом аммониевой соли.
По числу NH2 – групп в молекуле амины делят на моноамины, диамины и т.д.
|
из
5.00
|
Обсуждение в статье: Методы получение простых эфиров |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

