 |
Главная |
Линейчатый спектр атома водорода
|
из
5.00
|
Еще в начале 19 века опытным путем было установлено, что изолированные атомы в виде разреженного газа или паров металлов испускают спектр, состоящий из отдельных (дискретных) спектральных линий (линейчатый спектр).
Закономерности в спектральных линиях в видимой части спектра атома водорода были подробно изучены в 1885 г. швейцарским физиком Иоганном Бальмером.
Совокупность спектральных линий излучения атома водорода в видимой части спектра была названа серией Бальмера.
Длины волн в этой части спектра вычислялись по формуле:
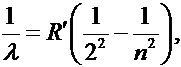
Где 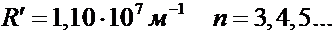
Позже аналогичные серии спектральных линий были обнаружены другими учеными в УФ и ИК частях спектра атома водорода.
В 1890 г. И. Ридберг получил эмпирическую обобщенную формулу для частот спектральных линий атома водорода:
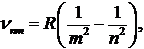
 Где
Где 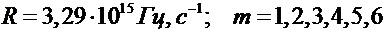 – постоянные для каждой серии целые числа,
– постоянные для каждой серии целые числа,
n – целые числа, начинающие с m+1, которые определяют отдельные линии в данной серии.
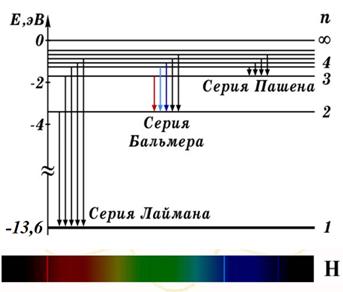
Для УФ серии Лаймана: m = 1, n = 2, 3, 4…;
Для серии Бальмера: m = 2, n = 3, 4, 5,…
Для ИК серии Пашена: m = 3, n = 4, 5, 6,…
До теории атома водорода Бора механизм происхождения линейчатых спектров и физический смысл целых чисел, входящих в формулы спектральных линий водорода, оставались непонятными.
Постулаты Бора
Первый постулат: атом может находиться в стационарных состояниях. Этим состояниям соответствуют дискретные орбиты электрона, находясь на которых электрон не излучает электромагнитных волн.
Условие для стационарных орбит элек-трона: момент импульса электрона должен быть равен целому кратному величине 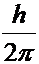 :
:
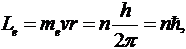
гдеn = 1, 2, 3, …называется главным квантовым числом.
Второй постулат: излучение или поглощение энергии в виде кванта энергии 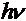 происходит лишь при переходе электрона из одного стационарного состояния в другое.
происходит лишь при переходе электрона из одного стационарного состояния в другое.
Световой квант равен разности энергий тех стационарных состояний, между которыми совершается квантовый скачок электрона:
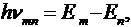
 гдеm и n – номера состояний.
гдеm и n – номера состояний.
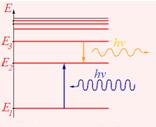
При 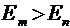 происходит излучение фотона (переход атома из состояния с большей энергией Е3 в состояние с меньшей энергией Е2).
происходит излучение фотона (переход атома из состояния с большей энергией Е3 в состояние с меньшей энергией Е2).
При 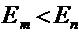 – его поглощение (переход электрона из состояния с меньшей энергией Е1 в состояние с большей энергией Е2)
– его поглощение (переход электрона из состояния с меньшей энергией Е1 в состояние с большей энергией Е2)
Вставка модели № 96244 «Второй постулат Бора»
Опыт Франка и Герца.
Почти одновременно с теоретическими исследованиями Бора по атому водорода было получено прямое экспериментальное доказательство существования стационарных состояний атома и квантования энергии.
Дискретность энергетических состояний атома была доказана в 1913 г. в опыте Д. Франка и Г. Герца, в котором исследовалось столкновение электронов с атомами ртути.
Оказалось, что если кинетическая энергия электронов меньше 4,9 эВ, то их столкновение с атомами ртути происходит по закону абсолютно упругого удара.
Если же энергия электронов равна 4,9 эВ, то их столкновения с атомами ртути становятся неупругими, т. е. в результате столкновения с атомами ртути электроны полностью теряют свою кинетическую энергию.
Это означает, что атомы ртути поглощают определенную порцию энергии электрона и переходят из основного состояния в первое возбужденное состояние:
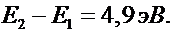
Согласно теории Бора, при обратном самопроизвольном переходе атома ртути в основное состояние должны испускаться кванты с частотой
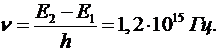
Спектральная линия с такой частотой действительно была обнаружена в УФ части спектра излучения атомов ртути.
Прекрасное согласие теории атома водорода Бора с экспериментом, вычисление постоянной Ридберга, объяснение наличия энергетических уровней у атома водорода служили вескими аргументами в пользу ее справедливости.
Однако теория Бора поставила перед физиками ряд еще более трудноразрешимых загадок:
- теория не могла объяснить различие интенсивности спектральных линий и причины тех или иных квантовых скачков;
- невозможность применить теорию для объяснения спектра гелия.
После открытия волновых свойств вещества стало совершенно ясно, что теория Бора, опирающаяся на классическую механику, могла быть только переходным этапом на пути к созданию последовательной квантовой теории атомных явлений.
|
из
5.00
|
Обсуждение в статье: Линейчатый спектр атома водорода |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

