 |
Главная |
Общее уравнение Шредингера. Уравнение Шредингера для стационарных состояний. Атом водорода в квантовой механике. Квантовые числа. Принцип Паули.
|
из
5.00
|
Уравнение Шредингера – основное уравнение квантовой механики – поз-воляет найти волновые функции ча-стиц, движущихся в различных сило-вых полях.
 в общем виде.
в общем виде.
Если силовое поле, в котором движется частица стационарно и функция U явно не зависит от времени, то уравнение Шредин-гера примет вид:
 ,
,
где Е – полная энергия частицы.
Для стационарных состояний при движе-нии частицы вдоль одной координатной оси X:

Оказалось, что состояние электрона в атоме водорода характеризуется определенным набором квантовых чисел.
Главное квантовое число n определяет энергетические уровни электрона в атоме и может принимать любые целочисленные значения начиная с единицы:
n = 1, 2, 3, …
Орбитальное квантовое число l , которое при заданном значении n может принимать значения
l = 0, 1, 3, …, (n – 1)
характеризует геометрию орбиты электро-на (ее эллиптичность) и определяет дис-кретный набор возможных значений меха-нического орбитального момента импульса электрона:
Из решения уравнения Шредингера сле-дует также, что вектор момента импульса электрона может иметь такие ориента-ции в пространстве, при которых его про-екция на направление z внешнего магнит-ного поля принимает квантованные значе-ния:
где – магнитное квантовое число, кото-рое при заданном l может принимать кван-тованные значения:
Таким образом, каждому значению глав-ного квантового числа n, определяющему энергетическое состояние атома, соответ-ствует ряд комбинаций квантовых чисел l и ml.
Каждой такой комбинации соответствует определенное распределение вероятности обнаружения электрона в различных точках пространства («электронное обла-ко»).
Квантовые числа n и l характеризуют размер и форму электронного облака, а кван-товое число ml – ориентацию элек-тронного облака в пространстве.
Число различных состояний, соответ-ствующих данному n, равно
Область пространства, в которой высока вероятность обнаружения электрона, назы-ваюторбиталью.
В квантовой механике принято называть состояния электрона, характеризующиеся квантовыми числами
l = 0 s-состояниями,
l = 1 – p-состояниями,
l = 2 – d-состояниями,
l = 3 – f-состояниями и т. д.
В 1925 г. швейцарский физик В. Паули от-крыл закон, известный под названием принцип Паули или принцип запрета:
в одном и том же атоме не может быть более одного электрона с одинаковым набором четырех квантовых чисел n, l, ml, ms.
 ,
,
где z – число электронов, находящихся в квантовом состоянии, опи-сываемых набором четырех квантовых чи-сел: 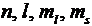 .
.
Строение атомного ядра. Модели ядра. Ядерные реакции. Радиоактивные превращения ядер. Реакция ядерного деления. Цепная реакция деления. Ядерный реактор. Термоядерный синтез. Управляемый термоядерный синтез.
Атом состоит из ядра и окружающего его электронного "облака". Находящиеся в электронном облаке электроны несутотрицательный электрический заряд. Протоны, входящие в состав ядра, несут положительный заряд.
В любом атоме число протонов в ядре в точности равно числу электронов в электронном облаке, поэтому атом в целом – нейтральная частица, не несущая заряда.
Атом может потерять один или несколько электронов или наоборот – захватить чужие электроны. В этом случае атом приобретает положительный или отрицательный заряд и называется ионом.
Практически вся масса атома сосредоточена в его ядре, так как масса электрона составляет всего лишь 1/1836 часть массы протона. Плотность вещества в ядре фантастически велика – порядка 1013 - 1014 г/см3. Спичечный коробок, наполненный веществом такой плотности, весил бы 2,5 миллиарда тонн!
Внешние размеры атома – это размеры гораздо менее плотного электронного облака, которое примерно в 100000 раз больше диаметра ядра.
Кроме протонов, в состав ядра большинства атомов входят нейтроны, не несущие никакого заряда. Масса нейтрона практически не отличается от массы протона. Вместе протоны и нейтроны называются нуклонами (от латинского nucleus – ядро).
Электроны, протоны и нейтроны являются главными "строительными деталями" атомов и называются субатомными частицами.
Модели ядра:
Капельная модель ядра– основана на аналогии между поведением нуклонов в ядре и молекул в капле жидкости:
– в обоих случаях – силы, действующие внутри капли и внутри ядра – короткодействующие и им свойственно насыщение;
– постоянная плотность вещества;
– объемы капли и ядра пропорциональны числу частиц.
Трудности: модель не смогла объяснить повышенную устойчивость ядер, содержащих магические числа протонов и нейтронов.
Оболочечная модель ядра предполагает распределение нуклонов в ядре по дискретным энергетическим уровням (оболочкам), заполняемым нуклонам согласно принципу Паули.
Экспериментально было установлено, что для самых стабильных ядер число протонов или число нейтронов равно одному из следующих целых чисел: 2, 8, 20, 50, 82, 126, …, которые называются магическими числами.
Эта модель объясняет:
–почему ядра с полностью заполненными оболочками (магические ядра) являются наиболее устойчивыми;
– спины и магнитные моменты ядер;
– различную устойчивость атомных ядер;
– периодичность изменения свойств атомных ядер.
Ядерная реакция – это процесс взаимодействия атомного ядра с другим ядром или элементарной частицей, сопровождающийся изменением состава и структуры ядра и выделением вторичных частиц или 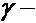 квантов.
квантов.

При ядерных реакциях выполняются несколькозаконов сохранения: энергии, электрического заряда, импульса, момента импульса и ряд других законов сохранения, специфических для физики элементарных частиц.
Ядерные реакции сопровождаются энергетическими превращениями.
Энергетическим выходом ядерной реакции называется величина

где  – сумма масс частиц, вступающих в ядерную реакцию,
– сумма масс частиц, вступающих в ядерную реакцию, 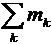 – сумма масс образующихся частиц.
– сумма масс образующихся частиц.
Ядерные реакции могут протекать с выделением тепла (экзотермические Q> 0) и с поглощением тепла (эндотермические Q< 0).
Для того, чтобы ядерная реакция имела положительный энергетический выход, удельная энергия связи нуклонов в ядрах исходных продуктов должна быть меньше удельной энергии связи нуклонов в ядрах конечных продуктов.
Как уже отмечалось выше, возможны два принципиально различных способа освобождения ядерной энергии:
1. Деление тяжелых ядер – процесс, при котором нестабильное ядро делится на два крупных ядра сравнимых масс.
2. Ядерный синтез – т. е. слияние легких ядер в одно ядро. Эти реакции носят название термоядерные реакции, т. к. для синтеза ядер необходимы очень высокие температуры.
Рассмотрим каждый тип этих реакций подробнее.
|
из
5.00
|
Обсуждение в статье: Общее уравнение Шредингера. Уравнение Шредингера для стационарных состояний. Атом водорода в квантовой механике. Квантовые числа. Принцип Паули. |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

