 |
Главная |
Основания. Классификация и химические свойства оснований. Примеры?
|
из
5.00
|
Основания – это сложные вещества, состоящие из атомов металлов и одной или нескольких гидроксогрупп (ОН-). С точки зрения теории электролитической диссоциации — это электролиты (вещества, растворы или расплавы которых проводят электрический ток), диссоциирующие в водных растворах на катионы металлов и анионы только гидроксид - ионов ОН-. Растворимые в воде основания называются щелочами. К ним относятся основания, которые образованы металлами 1-й группы главной подгруппы (LiOH, NaOH и другие) и щелочноземельными металлами (Са(ОН)2, Sr(ОН)2, Ва(ОН)2). Основания, образованные металлами других групп периодической системы в воде, практически не растворяются. Щелочи в воде диссоциируют полностью: NaOH Na+ + OH-. Многокислотные основания в воде диссоциируют ступенчато: Ba(OH)2 BaOH+ + OH-, Ba(OH)+ 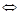 Ba2+ + OH-. Cтупенчатой диссоциацией оснований объясняется образование основных солей. Основания называются следующим образом: сначала произносят слово «гидроксид», а затем металл, который его образует. Если металл имеет переменную валентность, то она указывается в названии. КОН – гидроксид калия; Ca(OH)2 – гидроксид кальция; Fe(OH)2 – гидроксид железа (II); Fe(OH)3 – гидроксид железа (III); Классификация оснований по следующим признакам: 1. По кислотности (по числу групп ОН— в молекуле основания): однокислотные – NaOH, KOH, многокислотные – Ca(OH)2, Al(OH)3. 2. По растворимости: растворимые (щелочи) – LiOH, KOH, нерастворимые – Cu(OH)2, Al(OH)3. 3. По силе (по степени диссоциации): а) сильные (α = 100 %) – все растворимые основания NaOH, LiOH, Ba(OH)2, малорастворимый Ca(OH)2. б) слабые (α < 100 %) – все нерастворимые основания Cu(OH)2, Fe(OH)3 и растворимое NH4OH. 4. По химическим свойствам: основные – Са(ОН)2, NaОН; амфотерные – Zn(ОН)2, Al(ОН)3. Основания. Это гидроксиды щелочных и щелочноземельных металлов (и магния), а также металлов в минимальной степени окисления (если она имеет переменное значение). Например: NaOH, LiOH, Mg(OH)2, Ca(OH)2, Cr(OH)2, Mn(OH)2. Получение 1. Взаимодействие активного металла с водой: 2Na + 2H2O → 2NaOH + H2
Ba2+ + OH-. Cтупенчатой диссоциацией оснований объясняется образование основных солей. Основания называются следующим образом: сначала произносят слово «гидроксид», а затем металл, который его образует. Если металл имеет переменную валентность, то она указывается в названии. КОН – гидроксид калия; Ca(OH)2 – гидроксид кальция; Fe(OH)2 – гидроксид железа (II); Fe(OH)3 – гидроксид железа (III); Классификация оснований по следующим признакам: 1. По кислотности (по числу групп ОН— в молекуле основания): однокислотные – NaOH, KOH, многокислотные – Ca(OH)2, Al(OH)3. 2. По растворимости: растворимые (щелочи) – LiOH, KOH, нерастворимые – Cu(OH)2, Al(OH)3. 3. По силе (по степени диссоциации): а) сильные (α = 100 %) – все растворимые основания NaOH, LiOH, Ba(OH)2, малорастворимый Ca(OH)2. б) слабые (α < 100 %) – все нерастворимые основания Cu(OH)2, Fe(OH)3 и растворимое NH4OH. 4. По химическим свойствам: основные – Са(ОН)2, NaОН; амфотерные – Zn(ОН)2, Al(ОН)3. Основания. Это гидроксиды щелочных и щелочноземельных металлов (и магния), а также металлов в минимальной степени окисления (если она имеет переменное значение). Например: NaOH, LiOH, Mg(OH)2, Ca(OH)2, Cr(OH)2, Mn(OH)2. Получение 1. Взаимодействие активного металла с водой: 2Na + 2H2O → 2NaOH + H2 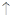 Ca + 2H2O → Ca(OH)2 + H2
Ca + 2H2O → Ca(OH)2 + H2  2. Взаимодействие основных оксидов с водой (только
2. Взаимодействие основных оксидов с водой (только  для щелочных и щелочноземельных металлов): Na2O + H2O → 2NaOH, CaO + H2O → Ca(OH)2. 3. Промышленным
для щелочных и щелочноземельных металлов): Na2O + H2O → 2NaOH, CaO + H2O → Ca(OH)2. 3. Промышленным 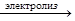 способом получения щелочей является электролиз растворов солей: 2NaCI + 4H2O
способом получения щелочей является электролиз растворов солей: 2NaCI + 4H2O  2NaOH + 2H2 + CI2
2NaOH + 2H2 + CI2 
4. Взаимодействие растворимых солей со щелочами, причем для нерастворимых оснований это единственный способ получения: Na2SO4 + Ba(OH)2 → 2NaOH + BaSO4  MgSO4 + 2NaOH → Mg(OH)2
MgSO4 + 2NaOH → Mg(OH)2  + Na2SO4.
+ Na2SO4.
5. Взаимодействие с некоторыми простыми веществами (амфотерными металлами, кремнием и другими):
2NaOH + Zn + 2H2O → Na2[Zn(OH)4] + H2  ; 2NaOH + Si + H2O → Na 2SiO3 + 2H2
; 2NaOH + Si + H2O → Na 2SiO3 + 2H2 
6. Взаимодействие с растворимыми солями с образованием осадков: 2NaOH + CuSO4 → Cu(OH)2  + Na2SO4,
+ Na2SO4,
7. Малорастворимые и нерастворимые основания разлагаются при нагревании: Ca(OH)2 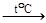 CaO + H2O,
CaO + H2O,
Амфотерные гидроксиды. Это гидроксиды металлов (Be(OH)2, AI(OH)3, Zn(OH)2) и металлов в промежуточной степени окисления (Сr(OH)3, Mn(OH)4). Амфотерные гидроксиды получают взаимодействием растворимых солей со щелочами взятых в недостатке или эквивалентном количестве, т.к. в избытке они растворяются: AICI3 + 3NaOH → AI(OH)3  +3NaCI. Амфотерные гидроксиды проявляют свойства оснований и кислот, поэтому взаимодействуют как с кислотами, так и с основаниями. 1. Взаимодействие с кислотами с образованием соли и воды: Zn(OH)2 + H2SO4 → ZnSO4 + 2H2O. 2. Взаимодействие с растворами и расплавами щелочей с образованием соли и воды:
+3NaCI. Амфотерные гидроксиды проявляют свойства оснований и кислот, поэтому взаимодействуют как с кислотами, так и с основаниями. 1. Взаимодействие с кислотами с образованием соли и воды: Zn(OH)2 + H2SO4 → ZnSO4 + 2H2O. 2. Взаимодействие с растворами и расплавами щелочей с образованием соли и воды:  AI(OH)3 + NaOH
AI(OH)3 + NaOH 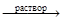 Na[AI(OH)4], AI(OH)3 + NaOH
Na[AI(OH)4], AI(OH)3 + NaOH 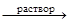 NaAIO2 + 2H2O. 3. Взаимодействие с кислотными и основными оксидами: 2Fe(OH)3 + 3SO3
NaAIO2 + 2H2O. 3. Взаимодействие с кислотными и основными оксидами: 2Fe(OH)3 + 3SO3 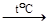
 Fe2(SO4)3 + 3H2O, 2Fe(OH)3 + Na2O
Fe2(SO4)3 + 3H2O, 2Fe(OH)3 + Na2O 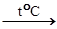 2NaFeO2 + 3H2O.
2NaFeO2 + 3H2O.
|
из
5.00
|
Обсуждение в статье: Основания. Классификация и химические свойства оснований. Примеры? |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

