 |
Главная |
Порядок выполнения работы
|
из
5.00
|
Растворы:
- хлороводорода (соляной кислоты) НСl ; сЭ = 1 моль/л;
- пероксида водорода (перекиси водорода) Н2О2; сЭ = 1 моль/л;
- тиосульфата натрия Na2S2O3 ; сЭ = 1 моль/л;
- йодида калия KI; сЭ = 1 моль/л;
- раствор крахмала.
Оборудование:
- мерные цилиндры;
- стаканчики;
- секундомер.
Зависимость скорости реакции от концентрации реагирующих веществ можно проследить на реакции (32) окисления йодида калия пероксидом водорода в кислой среде хлороводорода:
2 КI + Н2О2 + 2 НСl = 2 KCl + 2 H2O + I2 .
Эта реакция состоит из двух стадий:
1) Реакция разложения пероксида водорода с образованием атомарного кислорода:
 Н2О2 Н2О + О0 ,
Н2О2 Н2О + О0 ,
который окисляет затем иодид-ион в свободный йод:
0 -1 -2 0
 2) О + 2I O + I2 .
2) О + 2I O + I2 .
Выделившийся йод фиксируется крахмалом (посинение), имеющимся в растворе.
Кроме реакции (32) для наблюдения за скоростью используют реакцию с тиосульфатом натрия, восстанавливающим йод в иодид-ион;
2Na2S2O3 + I2 = 2 NaI + Na2S4O6 .
Обе реакции (32) и (33) проводят одновременно в одной реакционной смеси. Так как реакция (33) протекает быстрее реакции (32), то свободный йод появляется в растворе только после полного окисления всего тиосульфата натрия. Скорость суммарного процесса последовательных реакций определяется первой (более медленной) стадией.
В химических стаканчиках готовятся: раствор №1 (смешиванием растворов пероксида водорода, хлороводорода и крахмала) и раствор №2 (смешиванием растворов иодида калия и тиосульфата натрия). Объёмы растворов отмериваются мерными цилиндрами по данным таблицы 2.
Приготовленные растворы №1 и №2 сливают в один стаканчик и ведут отсчёт времени по секундомеру до появления синей окраски раствора. Она не появляется в растворе до тех пор, пока не будет полностью окислен йодом тиосульфат натрия. После окончания реакции (33) - йода с тиосульфатом натрия, первые порции выделившегося йода окрашивают раствор в синий цвет. Отсчет времени ( 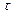 ) ведут с момента сливания растворов №1 и №2 в один стаканчик до появления синей окраски раствора.
) ведут с момента сливания растворов №1 и №2 в один стаканчик до появления синей окраски раствора.
По данным таблицы 2 видно, что в ходе опытов изменяют концентрацию Н2О2 , добавляя к раствору №1 разное количество воды. Видно также, что общий объем реакционной смеси в каждом опыте одинаков и составляет 60 мл. Следовательно, концентрации пероксида водорода в реакционной смеси растут от опыта к опыту, и их величины соотносятся между собой, как номера опытов 1:2:3:4:5. Объём раствора крахмала в каждом опыте одинаков и составляет 1-2 мл.
Результаты записывают в таблицу и делают вывод о зависимости скорости реакции от концентрации.
Таблица 2
Состав растворов для опытов
|
№1 опыта | Раствор №1 | Раствор №2 |
| |||
| 0,2 н H2O2 V, мл. | Н2О V, мл | 1 н HCl V, мл. | 0,25 н KI V, мл | 0,01 н NaS2O3 V. мл | ||
| 1 2 3 4 | 5 10 15 20 | 15 10 5 - | 10 10 10 10 | 15 15 15 15 | 15 15 15 15 | |
Контрольные вопросы
1. Что называется скоростью химических реакций (дайте определение)?
2. Какие реакции являются гомогенными и гетерогенными?
3. Какие факторы влияют на скорость реакции?
4. Как описывается зависимость скорости реакции от концентрации реагирующих веществ?
5. Напишите выражение закона действующих масс для реакций:
N2(г) + 3Н2(г) Û 2NН3(г);
2NO(г) + О2(г) Û 2NO2(г) ;
Ств +О2(г) Û СО2(г).
6. От чего зависит константа скорости реакции?
7. Каков физический смысл константы скорости реакции?
8. Приведите примеры простых и сложных реакций.
9. Какие реакции называются обратимыми?
10. Приведите примеры параллельных реакций
11. Какие реакции называются последовательными?
|
из
5.00
|
Обсуждение в статье: Порядок выполнения работы |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы


 , с
, с