 |
Главная |
Механический принцип относительности 1 страница
|
из
5.00
|
Во всех инерциальных системах отсчета при одних и тех же условиях все механические явления протекают одинаково.
Краткое теоретическое обоснование
механического принципа относительности
Этот принцип называется также механическим принципом относительности или принципом относительности Галилея; сформулирован Г.Галилеем в 1636 г. в книге «Диалог о двух главнейших системах мира ‑ птолемеевой и коперниковой»; является обобщением опыта и подтверждается многообразием приложений классической механики к движению тел и может быть сформулирован так: никакими механическими опытами, проводящимися в какой-либо ИСО, нельзя определить, покоится данная система или движется равномерно и прямолинейно.
Например, находясь в каюте корабля, движущегося равномерно и прямолинейно, невозможно, не выглянув в иллюминатор, определить, покоится корабль или движется.
Сам принцип логически следует из известных преобразований Галилея.
Преобразованиями Галилея называются преобразования координат и времени, применяемые в классической механике при переходе от одной инерциальной системы отсчета к другой, которая движется относительно первой поступательно и с постоянной скоростью.
В простейшем двумерном случае преобразования Галилея имеют следующий вид (рис. 1):  =
=  * +
* +  =
=  * +
* +  t,
t,
t = t * ,
где  – радиус-вектор движущейся точки М относительно «неподвижной» системы отсчета {x , y};
– радиус-вектор движущейся точки М относительно «неподвижной» системы отсчета {x , y};  *– радиус-вектор точки М в движущейся системе{x * , y *};
*– радиус-вектор точки М в движущейся системе{x * , y *};  =
=  t – радиус-вектор, соединяющий начала координат систем отсчета;
t – радиус-вектор, соединяющий начала координат систем отсчета;  – скорость поступательного прямолинейного равномерного движения системы {x * , y*} относительно системы {x , y}. Или в координатной форме: x = x * + Ut , y = y,* t = t*.
– скорость поступательного прямолинейного равномерного движения системы {x * , y*} относительно системы {x , y}. Или в координатной форме: x = x * + Ut , y = y,* t = t*.

Рис. 1.
Эти преобразования справедливы лишь при скоростях много меньше скорости света в вакууме (V << c) и основываются на двух предположениях, которые принимались неявно и считались очевидными:
- ход времени одинаков во всех инерциальных системах отсчета;
- линейные размеры тела не зависят от скорости его движения относительно системы отсчета.
Из преобразований Галилея следуют:
- классический закон сложения скоростей:  =
=  * +
* + 
где  – скорость точки М в «неподвижной» системе отсчета {x , y},
– скорость точки М в «неподвижной» системе отсчета {x , y},  * – скорость точки М в движущейся системе {x * , y *};
* – скорость точки М в движущейся системе {x * , y *};
- инвариантность[55] ускорения точки М и сил, действующих на неё:
 =
=  *;
*;  =
=  *.
*.
Из последних соотношений следует, что уравнение второго закона Ньютона не изменяется при переходе от одной ИСО к другой, т.е. законы Ньютона инвариантны к преобразованиям Галилея.
Современные формулировки классического принципа относительности:
1) Во всех ИСО при одних и тех же условиях все механические явления протекают одинаково.
2) Законы классической механики инвариантны относительно перехода их одной ИСО в другую.
В современной физике показано, что классический принцип относительности свидетельствует о том, что все ИСО равноправны, «абсолютной» системы отсчета нет.
Законы сохранения
Для замкнутых систем существуют такие функции координат и скоростей тел (материальных точек) образующих систему, которые сохраняют при движении постоянные значения. Эти функции называются интегралами движения. Интегралы движения полезны потому, что некоторые свойства этого движения можно узнать даже без интегрирования уравнений движения.
В классической механике для замкнутой системы из N частиц, между которыми нет жёстких связей, можно образовать (6 N  интегралов движения. Из них аддитивными являются три: энергия , импульс , момент импульса.
интегралов движения. Из них аддитивными являются три: энергия , импульс , момент импульса.
Закон сохранения механической энергии
В инерциальной системе отсчёта полная механическая энергия замкнутой системы частиц, между которыми действуют только консервативные силы[56], остаётся постоянной: Е = T + U = const, где E – полная энергия механической системы, Т – её кинетическая энергия, U – её потенциальная энергия.
Закон сохранения механической энергии был впервые сформулирован Г.Лейбницем.
Закон сохранения импульса
В инерциальной системе отсчёта векторная сумма импульсов всех тел системы есть величина постоянная, если векторная сумма внешних сил, действующих на систему тел, равна нулю.
Закон сохранения импульса впервые был сформулирован Р. Декартом.
Закон сохранения момента импульса
В инерциальной системе отсчёта момент импульса замкнутой системы частиц не изменяется со временем.
В классической механике законы сохранения выводятся как следствие законов Ньютона. Однако эти законы далеко выходят за рамки ньютоновской механики, а справедливы для всей физики и принадлежат к самым фундаментальным законам природы. Фундаментальность законов сохранения связана, согласно теореме Нётер[57], с фундаментальными симметриями пространства и времени: закон сохранения энергии – с однородностью времени[58], закон сохранения импульса ‑ с однородностью пространства[59], закон сохранения момента импульса – с изотропностью пространства[60].
2.2.2. Термодинамическая картина мира как этап механической картины мира
2.2.2.1. Становление термодинамической картины мира (ТКМ)
Начало XIX в. ознаменовалось развитием теплотехники и теплоэнергетики, интенсивным внедрением парового двигателя в транспорт и промышленность. Освоение теплоэнергетики, появление самых разнообразных модификаций тепловых двигателей и их эксплуатация требуют глубокого знания тепловых процессов. Разрабатывается термодинамический подход к их изучению. Его становление связано с именами С.Карно[61], Р.Майера[62], Р.Клаузиуса[63], Г.Гельмгольца[64], В.Нернста[65] и др.
Первоначально термодинамика изучала тепловые свойства макроскопических систем, не вдаваясь в их микроскопическое строение. Ее основание составляли понятия температуры, теплоты, работы, энергии, теплоемкости, энтропии и три фундаментальных закона (начала), являвшиеся результатом обобщения огромного числа экспериментальных наблюдений. Первое и второе начала, по сути, устанавливают отношения между переданной системе теплотой и совершенной механической работой. Создавалось мнение, что термодинамика – это механическая теория теплоты.
Однако открытая термодинамикой необратимость тепловых процессов нарушила представления об однозначности их описания. И уже в работе Клаузиуса «Механическая теория тепла» появляется идея о статистическом характере тепловых законов. Одно из важнейших утверждений этой работы: поведение коллектива частиц носит вероятностный характер.
Приложение теории вероятности к термодинамическим системам явилось важной вехой в развитии физики. Прорыв в этой области сделал организатор и первый директор знаменитой Кавендишской лаборатории Д.Максвелл[66], который, используя классическую механику и представления о вероятности, получил закон распределения молекул по скоростям, показал, что в газовых средах, где преобладает хаотичность движения частиц, есть определенный порядок. Развивая это направление, Л.Больцман[67] дал статистическое обоснование второго начала, выразил энтропию системы через вероятность, описал поведение закрытой термодинамической системы.
При разработке статистической механики идеального газа Д.Максвелл и Л.Больцман указали на принципиальное отличие поведения отдельной частицы и большой совокупности частиц. Если при описании одной макрочастицы можно определить её координаты и скорости в любой момент времени, то при описании поведения большого коллектива частиц можно лишь указать распределение частиц в зависимости от какого-либо параметра (например, распределение молекул газа по скоростям, или распределение по высоте над уровнем моря плотности воздуха в атмосфере Земли). Закономерности этих распределений как целого есть результат хаотического движения частиц. С работами Максвелла и Больцмана закладываются основы нового направления ‑ статистической физики, которая основывается на атомистике и вероятности. В науке появляется представление о фундаментальности случайного и вероятностном характере причинно-следственных отношений. Эти идеи стали основополагающими для развития науки.
2.2.2.2. Фундаментальные представления термодинамической картины мира
1) Представления о материи, движении, пространстве и времени, взаимодействии и причинности в термодинамической картине мира остались такими же, как и в классической механике.
2) Представления о закономерности были частично изменены, а именно, допускается существование наряду с динамическими статистических законов, которые, как полагали в XIX в., сводятся к более фундаментальным динамическим законам.
Термодинамика описывают поведение макроскопических систем (твердых, жидких и газообразных тел), состоящих из большого числа частиц. В её основе лежат фундаментальные законы (начала), которые являются обобщением многочисленных наблюдений. Обоснование законов термодинамики, их связь с законами движения частиц, составляющих тела, дается статистической физикой, в которой свойства макроскопических систем (тел) выражаются через свойства этих частиц и их взаимодействия и описываются статистическими законами.
В статистических законах предсказания носят не строго определённый, а вероятностный характер. Подобный характер предсказаний обусловлен действием множества случайных факторов, которые имеют место в статистических системах (например, большого числа молекул в газе). Поэтому статистическая закономерность характеризует не столько поведение отдельного элемента, сколько коллектива в целом. Необходимость, проявляющаяся в статистических законах, возникает вследствие взаимной компенсации и уравновешивания множества случайных факторов.
Статистическая механика нарушала традиции классического описания физической реальности[68], ибо идеалом классического описания считалась динамическая детерминированная форма законов физики. Поэтому первоначально физики негативно относились к статистическим (вероятностным) законам, связывая их с мерой нашего незнания. Однако это не так. Статистические законы также выражают необходимые связи в природе. Действительно, во всех фундаментальных статистических теориях состояние представляет собой вероятностную характеристику системы, её уравнения движения по-прежнему определяют состояние (статистическое распределение) в любой последующий момент времени по заданному распределении в начальный момент.
Главное различие между динамическими и статистическими законами с философско-методологической точки зрения состоит в том, что в статистических законах необходимость выступает в диалектической связи со случайностью, а в динамических – как абсолютная противоположность случайного. А отсюда вывод: «Динамические законы представляют собой первый низший этап в процессе познания окружающего нас мира, статистические законы обеспечивают более современное отображение объективных связей в природе: они выражают следующий, более высокий этап познания».
3) Классическая термодинамика XIX в. называлась равновесной термодинамикой, т.к. изучала не существующие в реальности (т.е. идеальные) изолированные[69] макроскопические системы в равновесном состоянии[70].
В связи с вышеизложенным термодинамическую картину мира нельзя рассматривать как самостоятельную картину мира, а лишь как второй этап МКМ.
2.1.2.3. Содержание термодинамической картины мира
1). Структура термодинамики как научной теории
Основу ТКМ составили основные принципы (начала) и, как в МКМ,– атомизм (молекулярно-кинетическая теория строения вещества). Поэтому ТКМ использует взаимодополняющие друг друга термодинамический и статистический методы.
2). Термодинамический метод
Термодинамика изучает макроскопические процессы в телах, а именно, наиболее общие закономерности преобразования энергии, не рассматривая внутреннее строение тел. Её выводы основаны на общих принципах (началах), являющихся обобщением опытных фактов. В этом смысле – термодинамика – феноменологическая теория.
Классическая термодинамика изучает равновесные состояния и квазистатические процессы. Такие состояния и процессы в реальности не существуют.
3). Статистический метод в молекулярной физике
Молекулярно-кинетическая теория ставит целью исследовать макроскопические свойства тел, которые непосредственно наблюдаются на опыте (давление, температура и т.п.), как суммарный результат действия молекул.
В МКТ термодинамические системы – системы, состоящие из большого числа частиц. Поэтому МКТ пользуется статистическим методом, интересуясь не движением отдельных молекул, а лишь средними величинами, которые характеризуют движение их огромной совокупности:
1). Средняя скорость: <  =
=  =
=  ,
,
где  -–скорость i-той молекулы, N– число молекул.
-–скорость i-той молекулы, N– число молекул.
2). Средняя квадратичная скорость: <  =
=  =
= 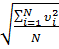 .
.
3). Средняя энергия: <  >=
>=  .
. 
Поэтому МКТ называют также статистической физикой.
В классической статистической физике молекулы рассматриваются как классические частицы, движение которых подчиняется законам классической механике, в т.ч. второму закону Ньютона.
Основным понятием статистической физики является функция распределения, характеризующая плотность вероятности распределения частиц статистической системы по фазовому пространству, т.е. по координатам qi и импульсам pi (например, функция f(  распределения Максвелла молекул идеального газа по скоростям).
распределения Максвелла молекул идеального газа по скоростям).
4). Основные положения молекулярно-кинетической теории строения вещества
Молекулярно-кинетической теорией (МКТ) называют учение о строении и свойствах вещества на основе представления о существовании атомов и молекул как наименьших частиц химических веществ.
Предположение о том, что любое вещество состоит из мельчайших неделимых частиц — атомов, было высказано около 2500 лет назад древнегреческими философами Левкиппом[71] и Демокритом[72]. По их представлениям все тела образуются в результате соединения атомов. Различия в свойствах тел объясняются тем, что тела состоят из различных атомов или одинаковые атомы по-разному соединены между собой в пространстве .Существенный вклад в развитие молекулярно-кинетических представлений сделал в середине XVIII в. великий русский ученый М.В.Ломоносов[73]. Он объяснил основные свойства газа, предположив, что все молекулы газа движутся беспорядочно, хаотично и при столкновениях отталкиваются друг от друга. Беспорядочным движением молекул М. В. Ломоносов впервые объяснил природу теплоты. В начале XIX столетия английский ученый Д. Дальтон[74] показал, что многие закономерности явлений природы можно объяснить, используя представления об атомах и молекулах, и научно обосновал молекулярное строение вещества. К началу ХХ столетия была окончательно создана и подтверждена множеством опытов молекулярно-кинетическая теория строения вещества.
В основе МКТ лежат три основных положения:
1. Все вещества – жидкие, твердые и газообразные – образованы из мельчайших частиц – молекул, которые сами состоят из атомов.
2. Между частицами вещества существуют силы взаимодействия – притяжения и отталкивания. Эти силы действуют на небольших расстояниях.
МКТ стала одной из самых успешных физических теорий и была подтверждена целым рядом опытных фактов. Основными доказательствами положений МКТ стали:
· диффузия
· броуновское движение
· изменение агрегатных состояний вещества.
На основе МКТ развит целый ряд разделов современной физики, в частности, физическая кинетика и статистическая механика. В этих разделах физики изучаются не только молекулярные (атомные или ионные) системы, находящиеся не только в «тепловом» движении, и взаимодействующие не только через абсолютно упругие столкновения. Термин же молекулярно-кинетическая теория в современной теоретической физике уже практически не используется, хотя он встречается в учебниках по курсу общей физики.
5). Основные структурные элементы термодинамики
1) Опытные факты
Рубежными экспериментами в становлении классической термодинамики стали опыты Бойля[75], Мариотта[76] и Гей-Люссака[77](конец XVIII в.), заложившие основы кинетической теории газов и позволившие дать фундаментальное определение температуры. Газовые законы составили начало предмета термодинамики.
Этапными экспериментами, опровергшими «теорию теплорода»[78] и приведшими к современной теории теплоты стали также опыты Румфорда[79](обратил внимание на повышение температуры металла при сверлении пушечных стволов), Дэви[80] (плавление льда при трении) и Джоуля[81] (установил количественно соотношение между теплотой и механической энергией).
В 1827 г. ботаник Броун[82] наблюдал беспорядочное движение частиц цветочной пыли, взвешенных в воде. Явление было объяснено в 1876 г. Рамзаем[83] и получило название «броуновское движение»[84].
Эти опыты и стали экспериментальной основой молекулярно-кинетической теории строения вещества.
2) Модели
Термодинамика, как и классическая механика, использует ряд модельных представлений: идеальный газ, изолированная термодинамическая система, идеальный тепловой двигатель, адиабатный процесс и т.д.
Идеальный газ — математическая модель газа , в которой в рамках молекулярно-кинетической теории предполагается, что: 1) потенциальной энергией взаимодействия частиц, составляющих газ, можно пренебречь по сравнению с их кинетической энергией; 2) суммарный объём частиц газа пренебрежимо мал; 3) между частицами нет дальнодействующих сил притяжения или отталкивания, соударения частиц между собой и со стенками сосуда абсолютно упруги ; 4) время взаимодействия между частицами пренебрежимо мало по сравнению со средним временем между столкновениями.
Изолированная система (замкнутая система) ‑ термодинамическая система, которая не обменивается с окружающей средой ни веществом, ни энергией.
Теплово́й дви́гатель — устройство, совершающее работу за счет использования внутренней энергии, тепловая машина, превращающая тепло в механическую энергию, использует зависимость теплового расширения вещества от температуры. В основу работы идеального теплового двигателя, имеющего максимально возможный КПД, положен термодинамический цикл Карно.
Адиабати́ческий (адиаба́тный) проце́сс — термодинамический процесс в макроскопической системе, при котором система не обменивается теплотой с окружающим пространством.
3) Физические величины
Физические величины, характеризующие термодинамическое состояние системы называются термодинамическими параметрами. Основными термодинамическими параметрами являются объём V, давление Р и температура Т.
Ключевыми понятиями ТКМ являются понятие «количество теплоты»  ‑ количество энергии, переданное системе внешними телами путём теплообмена; «внутренняя энергия» U ‑ энергия хаотического (теплового) движения микрочастиц системы (молекул, атомов, электронов, ядер и т.п.) и энергия взаимодействия этих частиц, однозначная функция состояния термодинамической системы и «энтропия»
‑ количество энергии, переданное системе внешними телами путём теплообмена; «внутренняя энергия» U ‑ энергия хаотического (теплового) движения микрочастиц системы (молекул, атомов, электронов, ядер и т.п.) и энергия взаимодействия этих частиц, однозначная функция состояния термодинамической системы и «энтропия»  (от др.греч. ἐντροπία — поворот, превращение) — функция состояния термодинамической системы , определяющая меру необратимого рассеивания энергии, в статистической физике — мера вероятности осуществления какого-либо макроскопического состояния.
(от др.греч. ἐντροπία — поворот, превращение) — функция состояния термодинамической системы , определяющая меру необратимого рассеивания энергии, в статистической физике — мера вероятности осуществления какого-либо макроскопического состояния.
4) Исходные принципы термодинамики
В основе термодинамики лежат три основных закона, установленных на основе обобщения большого количества опытных фактов, называемых началами термодинамики.
Первое начало термодинамики было сформулировано в середине XIX века в результате работ немецкого учёного Ю. Р. Майера[85], английского физика Д. Джоуля и немецкого физика Г. Гельмгольца[86]:
Теплота, сообщаемая системе, расходуется на увеличение её внутренней энергии и на совершение работы ею против внешних сил :
 = dU +
= dU + 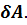
Первое начало термодинамики выражает закон сохранения энергии для термодинамических систем.
Второе начало термодинамики отражает направленность естественных процессов и налагает ограничения на возможные направления энергетических превращений в макроскопических системах, указывая, какие процессы в природе возможны, а какие – нет.
Математическим выражением второго начала термодинамики является принцип возрастания энтропии: энтропия замкнутой системы при любых, происходящих в ней процессах не убывает: dS  0.
0.
Необратимые процессы приводят к установлению равновесного состояния. В этом состоянии энтропия изолированной системы достигает максимума. Никакие макроскопические процессы в такой системе невозможны.
Так как все реальные процессы необратимые, то все процессы в замкнутой системе ведут к увеличению её энтропии.
Третье начало термодинамики (теоремы Нернста[87]) устанавливает абсолютное значение энтропии: энтропия любого тела стремиться к нулю при стремлении к абсолютному нулю его температуры:  = 0.
= 0.
5) Следствия
Из основных принципов (начал) термодинамики следует ряд выводов, имеющих большое теоретическое и практическое значение:
· о невозможности вечных двигателей первого[88] и второго[89] рода;
· наибольший КПД тепловой машины, работающей по циклу Карно, не зависит от рода рабочего тела и вполне определяется предельными температурами, между которыми машина работает.
· КПД необратимой тепловой машины всегда меньше, чем обратимой, работающей в аналогичных условиях (т.е. с теми же нагревателем и холодильником). Снижение КПД реальных тепловых машин по сравнению с теоретическим вызвано необратимыми процессами, которые происходят в самой машине (теплопроводностью и т.п.).
· пути повышения КПД тепловых машин: устранение (по мере возможности) и ослабление необратимых процессов. Если необратимый процесс всё же произошёл, то нет никакой возможности устранить его последствия, ведущие к ухудшению работы двигателя.
6). Второе начало термодинамики и «тепловая смерть Вселенной»
Вселенная - весь мир, безграничный во времени и пространстве и бесконечно разнообразный по тем формам, которые принимает материя в процессе своего развития.
На современном этапе существования (13,72 млрд. лет) Вселенная излучает как абсолютно чёрное тело с температурой 2,725 К. Максимум спектра излучения приходится на частоту 160,4 ГГц (микроволновое излучение), что соответствует длине волны 1,9 мм. Оно изотропно с точностью до 0,001 %.
Тепловая смерть — термин, описывающий конечное состояние любой замкнутой термодинамической системы , и Вселенной в частности. При этом никакого направленного обмена энергией наблюдаться не будет, так как все виды энергии перейдут в тепловую. Термодинамика рассматривает систему, находящуюся в состоянии тепловой смерти, как систему, в которой термодинамическая энтропия максимальна.
Вывод о «тепловой смерти» Вселенной был сформулирован Р. Клаузиусом в 1865 г. на основе второго начала термодинамики. Согласно второму началу термодинамики, любая физическая система, не обменивающаяся энергией с другими системами (для Вселенной в целом такой обмен, возможно, исключен), стремится к наиболее вероятному равновесному состоянию с максимумом энтропии. Такое состояние соответствовало бы «тепловой смерти» Вселенной.
Второе начало термодинамики иногда используется критиками эволюции с целью показать, что развитие природы в сторону усложнения невозможно. Подобная интерпретация физического закона неверна: ведь энтропия не убывает только в замкнутых системах.
Ещё до создания современной космологии были сделаны многочисленные попытки опровергнуть вывод о тепловой смерти Вселенной. Наиболее известна из них флуктуационная гипотеза Л. Больцмана (1872 г.), согласно которой Вселенная извечно пребывает в равновесном изотермическом состоянии, но по закону случая то в одном, то в другом её месте иногда происходят отклонения от этого состояния; они происходят тем реже, чем большую область захватывают и чем значительнее степень отклонения.
|
из
5.00
|
Обсуждение в статье: Механический принцип относительности 1 страница |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

