 |
Главная |
При этом происходит реакция:
|
из
5.00
|
Ag 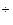 + CI
+ CI  ® AgCI
® AgCI
AgCI + 2NH  OH ® [Ag(NH3)
OH ® [Ag(NH3)  ]CI + 2H
]CI + 2H  O
O
[Ag(NH 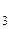 )
) 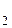 ]CI +2HNO3 ® AgCI + 2NH
]CI +2HNO3 ® AgCI + 2NH  NO
NO 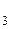
Опыт № 15. Реакция иона I–
Нитрат серебра образует с ионами йода желтый осадок йодида серебра, который не растворяется в воде, кислотах и в избытке аммиака.
Налейте в пробирку 2-3 капли раствора нитрата серебра, добавьте 2-3 капли йодида калия. Проверьте растворимость образованного осадка в аммиаке.
При этом происходит реакция:
Ag 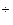 + І
+ І  ® AgІ
® AgІ
Опыт № 16. Реакция иона S2-
В пробирку с 1-2 каплями сульфида натрия добавьте 2-3 капли нитрата серебра. Проверьте растворимость осадка, образовавшегося в разбавленной азотной кислоте при нагревании.
При этом происходит реакция:
Ag 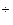 + S2
+ S2  ® Ag2S
® Ag2S
Опыт № 17. Реакция иона SO42-
Налейте в пробирку 3-4 капли раствора сульфата натрия и добавьте к нему 2-3 капли раствора хлорида бария. Проверьте растворимость осадка, образовавшегося в азотной кислоте.
При этом происходит реакция:
Ba2+ + SO42- ® BaSO4
Опыт № 18. Реакция иона CO32-
Налейте в две пробирки 3-4 капли раствора карбоната натрия и добавьте 2-3 капли хлорида бария. Проверьте растворимость осадка, который образовался, в соляной кислоте.
При этом происходит реакция:
BaCI  + Na2CO
+ Na2CO 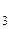 ® BaCO
® BaCO 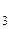 + 2NaCI
+ 2NaCI
Ba  + CO
+ CO 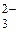 ® BaCO
® BaCO 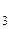
Задания для самостоятельной работы
Разобрать теоретический материал по теме «Основы качественного анализа», оформить лабораторной журнал, подготовиться к ответу на контрольные вопросы.
Контрольные вопросы:
1. Что лежит в основе аналитической классификации катионов по группам?
2. Приведите уравнение реакции взаимодействия катиона Pb2+, Al3+, Cu2+, Fe3+ с избытком раствора щелочи.
3. Как классифицируют анионы?
4. Какие анионы проявляют свойства окислителей?
5. Каким анионам характерные восстанавливающие свойства?
ОСНОВЫ КОЛИЧЕСТВЕННОГО АНАЛИЗА.
ГРАВИМЕТРИЧЕСКИЕ (ВЕСОВОЙ) АНАЛИЗ
ЛАБОРАТОРНАЯ РАБОТА № 7 (а)
ОПРЕДЕЛЕНИЕ КРИСТАЛЛИЗАЦИОННОЙ ВОДЫ В МЕДНОМ КУПОРОСЕ
(для студентов ТКДН, ТЭТД)
Цель работы: практическое определение содержания воды и минеральных веществ в некоторых системах, проведение соответствующих вычисленийрезультатов исследования.
Оборудование и реактивы:
- электрическая плитка с закрытой спиралью;
- фарфоровый тигли;
- электронные весы;
- шпатель;
- эксикатор;
- щипцы тигельные;
- медный купорос CuSO4·Н2О.
Методика определения
1. Взвесьте тигель на весах с точностью до 0,01 г и запишите его массу в лабораторный журнал.
2. Насыпьте ложкой в тигель 1г CuSO4 ·Н2О, распределите его ровным слоем на дне тигля.
3. Поставьте тигель на огонь и прокалите его до тех пор, пока кристаллогидрат медного купороса голубого цвета не превратится в серый порошок безводной соли CuSO4.
4. Перенесите щипцами горячий тигель в эксикатор, после охлаждения тигля взвесьте его и запишите вес.
5. Вычислите массовую долю (в %) кристаллизационной воды и количество молекул воды в CuSO4·Н2О.
Вычисления результатов работы
1. Определение навески медного купоросаCuSO4 ·Н2О.
Вес тигля с CuSO4 ·Н2О г
Вес тигля пустого г
Вес CuSO4 ·Н2О г (а)
2. Определение веса безводной соли – CuSO4.
Вес тигля с безводной солью г
Вес тигля пустого г
Вес CuSO4 г (в)
3. Определение веса кристаллизационной воды.
Вес CuSO4·Н2О г (а)
Вес CuSO4 г (в)
Вес кристаллизационной воды г (с)
4. Вычисление содержания кристаллизационной воды в процентах
Вес кристаллогидрата (а) – 100 %
Вес кристаллизационной воды (с) – Х %
 .
.
5. Вычисление количества молекул воды в CuSO4·Н2О
Вес CuSO4 (в) – вес кристаллизационной воды (с)
Молярная масса CuSO4 (160) – Р

Число молекул воды 
6. Напишите формулу кристаллогидрата медного купороса.
ЛАБОРАТОРНАЯ РАБОТА № 7 (б)
ОПРЕДЕЛЕНИЕ ВЛАЖНОСТИ ПРОДУКТОВ ПИТАНИЯ
(для студентов ТКДП, ТЭТД)
Цель работы: практическое определение влажности пищевых продуктов, проведение соответствующих вычислений результатов исследования.
Оборудование и реактивы:
- электронные весы;
- сушильный шкаф;
- продукты питания (пшеничная мука или манная крупа);
- бюксы металлические с крышками длиной 20 мм и диаметром 48 мм;
- эксикатор;
- щипцы тигельные.
Методика определения
1. Влажность определяют в двух параллельных навесках.
2. Взвесьте пустой металлический бюкс на технохимических весах с точностью до 0,01 г и запишите его массу в таблицу.
3. Насыпьте шпателем в бюкс 5,00 г тщательно перемешанного продукта питания (пшеничной муки или манной крупы), распределите его ровным слоем на дне бюкса.
4. Закройте бюкс крышкой и поставьте его в эксикатор.
5. Перенесите быстро открытый бюкс с продуктом в сушильный шкаф, поставив его на снятую крышку, и прокаливайте его 40 минут при температуре 130 0С.
6. По окончании сушки достаньте бюксы с продуктом из шкафа тигельными щипцами, закройте крышкой и перенесите в эксикатор для полного охлаждения, примерно на 20 минут. Взвесьте после этого бюкс с точностью 0,01 г и запишите результат в таблицу.
7.
Таблица 7.1 – Результаты исследования
| № | № бюкса | Масса пустого бюкса, г | Масса бюкса с продуктом до высушивания, г | Масса продукта m1 до высушивания, г | Масса бюкса с продуктом после высушивания, г | Массапродукта m2 после высушивания, г |
| 1 | ||||||
| 2 |
8. Вычислите влажность продукта питания (Х) по формуле:
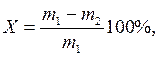

где m1 – масса пищевого продукта до высушивания, г
m2 – масса пищевого продукта после высушивания, г
9. Сравните полученные результаты с требованиями нормативного документа. Сделайте выводы о соответствии продукта питания нормативному документу (ГОСТ 26312.7-88 и ГОСТ 9404-88)
|
из
5.00
|
Обсуждение в статье: При этом происходит реакция: |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

