 |
Главная |
Токообразующей реакции
|
из
5.00
|
Токообразующей реакцией называется та окислительно-восстановительная реакция, которая самопроизвольно протекает в гальваническом элементе.
Например, в элементе Даниэля –Якоби:
 (–) Zn½ZnSO4 CuSO4 ½Cu (+)
(–) Zn½ZnSO4 CuSO4 ½Cu (+)
|
 Zn0 ® Zn2+ + 2
Zn0 ® Zn2+ + 2 
 Cu2+ + 2
Cu2+ + 2  ® Cu0
® Cu0
Zn0+ + Cu2+ ® Zn2+ + Cu0 токообразующая реакция
C помощью электрохимического метода могут быть рассчитаны следующие термодинамические характеристики:
а) Расчет изменения потенциала (DG).
Из раздела термодинамики известно, что
DG = –Wmax
Для электрохимической цепи максимальную электрическую работу характеризует величина
W = zFE,
где z – количество электронов, принимающих участие в реакции;
F – число Фарадея.
Следовательно, DG = zFE (7.78)
Это уравнение служит основой расчета DG различных химических реакций. Часто электрохимический метод определения изобарного потенциала имеет существенные преимущества передтермохимическим методом.
б) Расчет константы равновесия (Кр).
При стандартных условиях
DG0 = z F E0
Из термодинамики также известно, что

Следовательно,  (7.79)
(7.79)
Величина Кр характеризует полноту протекания химической реакции и вычисляется из уравнения:
 .
.
в) Расчет изменения энтропии (DS).
Из раздела термодинамики известно, что

Используя уравнение (7.6.1)
DG = – z FE,
находим, что 
Следовательно,  , (7.80)
, (7.80)
где  – температурный коэффициент, который показывает, как
– температурный коэффициент, который показывает, как
изменяется ЭДС при изменении температуры на 1 градус.
Для нахождения  надо измерить ЭДС при двух разных, но близких друг к другу температурах.
надо измерить ЭДС при двух разных, но близких друг к другу температурах.
ЭДС гальванической цепи зависит от температуры. Для одних цепей она увеличивается с повышением температуры, а для других – уменьшается. Изучение температурной зависимости гальванической цепи представляет большой интерес. Точное измерение самой ЭДС и ее температурного коэффициента  позволяет с большой точностью определить все важнейшие термодинамические характеристики токообразующей реакции, а именно: изменение изобарного потенциала (DG), энтальпии (DH) и энтропии системы (DS).
позволяет с большой точностью определить все важнейшие термодинамические характеристики токообразующей реакции, а именно: изменение изобарного потенциала (DG), энтальпии (DH) и энтропии системы (DS).
г) Расчет теплового эффекта реакции (DH).
К гальванической цепи, как и ко всякой химической и электрохимической системе, находящейся при постоянном давлении применимы все основные уравнения химической термодинамики, в том числе и уравнения Гиббса – Гельмгольца:
 ,
,
где DH – изменение энтальпии в ходе химической реакции.
Используя уравнения (7.6.1) и (7.6.3), получим
–z FE = DH – Tz F 
или DH = – z F  (7.81)
(7.81)
Следовательно, измерив ЭДС и взяв ее производную  (температурный коэффициент), можно определить теплоту токообразующей реакции, т.е. DH.
(температурный коэффициент), можно определить теплоту токообразующей реакции, т.е. DH.
Проведем анализ:
Если все члены уравнения Гиббса – Гельмгольца разделить на zF и поменять знаки, то с учетом формулы
Е = – 
получим следующее выражение:
Е = –  (7.82)
(7.82)
Как уже указывалось ранее
 ,
,
то  .
.
Таким образом, температурный коэффициент характеризует и изменение энтропии (DS) в ходе соответствующей химической реакции, а величина
zFT .  = T . DS
= T . DS
определяет тепловой эффект при обратимом протекании химической реакции в электрохимической системе.
С другой стороны, DH характеризует тепловой эффект химической реакции при ее необратимом протекании в условиях постоянного давления.
Будем рассматривать только самопроизвольно протекающие химические реакции, для которых Е > 0.
Такого вида электрохимические реакции протекают в гальванических элементах.
На опыте наблюдаются все три случая зависимости ЭДС от температуры
1.  = 0; ЭДС не зависит от температуры.
= 0; ЭДС не зависит от температуры.
2.  > 0; ЭДС растет с увеличением температуры.
> 0; ЭДС растет с увеличением температуры.
3.  < 0; ЭДС падает с ростом температуры.
< 0; ЭДС падает с ростом температуры.
Рассмотрим эти случаи с точки зрения соотношения электрической энергии и энергии химической реакции.
Если  = 0,
= 0,
то z FE = DH,
т.е. вся энергия, выделяющаяся при химической реакции, превращается в электрическую работу (W = zFE).
Если  < 0,
< 0,
то z F E = DH – z F E .  = DH – q,
= DH – q,
т. е. только часть энергии, выделяющейся при химической реакции, превращается в электрическую работу, а другая часть (q) выделяется в виде теплоты и элемент нагревается.
Наиболее интересен случай, когда  > 0.
> 0.
Тогда
z F E = DH + z F E .  = DH + q,
= DH + q,
т.е. электрическая работа больше энергии, выделяющейся при химической реакции на величину (q).
Дополнительная работа получается за счет теплоты, которую элемент отбирает от окружающей среды. Если система изолирована, то элемент охлаждается.
Таким образом, не имея разности температур, можно получить превращение теплоты в работу, т.е. протекает отрицательный процесс с уменьшением энтропии.
Приведите пример химического гальванического элемента, составленного из электрода первого рода и газового электрода, электрохимическая цепь с жидкостным соединением - «с переносом». Запишите уравнения электродных полуреакций, уравнение химической реакции, самопроизвольно протекающей в элементе, и уравнение Нернста для расчета ЭДС элемента
Цепь с переносом – это цепь с жидкостной границей. Например:

или
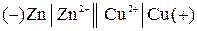 .
.
В состав электродов входят растворы различной природы или различной концентрации. Контакт между двумя растворами обеспечивается с помощью специальных приспособлений, например, солевым мостиком, состоящим из трубки, заполненной смесью влажного желеобразного вещества агар-агара с солью сильного электролита (КСl). Диффузионный потенциал на границе раздела раствор-раствор в этом случае устраняется.
Химические цепи с переносом. Уравнение Нернста для расчёта ЭДС гальванического элемента, составленного из газового и окислительно-восстановительного электродов. Влияние рН на ЭДС элемента.
Влияние рН на ЭДС элемента. 
|
из
5.00
|
Обсуждение в статье: Токообразующей реакции |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

