 |
Главная |
Зависимость скорости реакции от температуры
|
из
5.00
|
Необходимые исходные сведения и основные уравнения
Как правило, скорость химических реакций увеличивается при росте температуры. Этот рост в большинстве случаев подчиняется эмпирическому правилу Вант-Гоффа: при повышении температуры на каждые 10 оС скорость большинства реакций увеличивается в 2…4 раза. Температурный коэффициент скорости химической реакции g можно определить из отношения констант скоростей при двух разных температурах: k 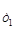 и k
и k  :
:
k  / k
/ k 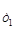 = g(T2-T1)/10. (4.1)
= g(T2-T1)/10. (4.1)
Экспериментальные данные показывают, что решение этого уравнения для подавляющего большинства химических реакций дает значение g, находящееся в интервале значений 2…4. По этой причине g носит название «температурный коэффициент повышения скорости химической реакции» или «коэффициент Вант-Гоффа».
Однако сам коэффициент Вант-Гоффа зависит от температуры и по этой причине уравнение 4.1 оказывается непригодным при расчете скорости реакций в широком интервале температур. Более точно зависимость константы скорости химической реакции от температуры описывается уравнением Аррениуса (в дифференциальной форме):
dlnk/dT = Eоп/RT2, (4.2)
где Еоп (или Еа) – энергия активации, Дж/моль.
После интегрирования получаем уравнение, пригодное для практических расчетов:
lgk2/k1 = Eоп.(T2−T1 ) / (2,3R . T1.T2)(4.3)
или k = k0 е-Еоп /RT ,(4.4)
где k0 – постоянная (предэкспоненциальный множитель).
Из уравнения (4.3) видно, что зависимость lgk от обратной температуры представляет собой прямую. Такая зависимость позволяет определять энергию активации и предэкспоненциальный множитель графически:
Eоп = 2,3.tga, (4.5)
где a - угол наклона прямой.
Задачи с решениями
1.При 25 оС некоторая реакция заканчивается за 3 часа. Принимая температурный коэффициент g равным 2,5, рассчи-тайте значение температуры, при котором реакция закончится в течение 30 мин.
Р е ш е н и е.Чем выше константа скорости, тем быстрее заканчивается реакция. Поэтому между этими величинами будет обратная зависимость: k  /k
/k  = t1/t2 = g(T2-T1)/10; 180/30=2,5(T2- 25). Т2 = 44,5 оС.
= t1/t2 = g(T2-T1)/10; 180/30=2,5(T2- 25). Т2 = 44,5 оС.
Ответ: Т2 = 44,5 оС.
2. Если проводить химическую реакцию между фиксированными концентрациями реагентов, период полураспада веществ зависит от температуры согласно нижеприведенной таблице:
| Температура, К | 798 | 813 | 828 | 843 | 858 | 873 |
| Период полураспада, с | 1072 | 631 | 380 | 229 | 144,5 | 89,1 |
Определите энергию активации реакции.
Решение. Допустим, что исходные вещества взяты в равных концентрациях. Тогда для реакции первого порядка t1/2 = = 0,693/ k , а для реакций второго порядка t1/2  . Для реакций третьего порядка аналогично. Подставив опытные данные в эти уравнения (независимо от порядка) и приравняв правые части уравнений, получим, что энергия активации равна 45,5 кДж/моль. Такое же значение получается и при других температурах.
. Для реакций третьего порядка аналогично. Подставив опытные данные в эти уравнения (независимо от порядка) и приравняв правые части уравнений, получим, что энергия активации равна 45,5 кДж/моль. Такое же значение получается и при других температурах.
Ответ: Еоп = 45,5 кДж/моль.
3. Скорость некоторой реакции изучалась в широкой области температур, и были найдены значения энергии активации при разных температурах:
| t, оС | 500 | 1000 | 1500 | 2000 | 2500 |
| Еа, кДж/моль | 48,0 | 46,0 | 44,0 | 42,1 | 40,1 |
Покажите, что полученные результаты согласуются с температурной зависимостью предэкспоненциального фактора в виде А = Т n и определите n.
Решение. Из данных видно, что Е = −4∙10-3. Поэтому зависимость энергии активации от температуры можно представить в виде уравнения (в интервале 500-2500 оС): Еа,Т = =50+(dE/dT)T. Например, при 1500 оС: Еа,1500= 50 – 4.10-3.1500 = = 44 кДж/моль.
Учитывая, что после логарифмирования и применения урав-нения Аррениуса получаем:
∆Т = nRT + T = Tопыт.
Таким образом, имеем два уравнения: Еоп – Е = nRT и Еоп – 50 = (dE/dT)Т
Следовательно, nR=dE/dT; n.2.10-3= −4.10-3 ; n = −2.
Зависимость предэкспоненциального фактора от температуры вытекает как из теории бинарных соударений, так и из теории активированного комплекса. В первой теории в предэкспоненту входит зависимость скорости движения молекул газа от температуры, во второй теории в этот же фактор входит зависимость статистических сумм вращательного и колебательного движения от температуры. Но так как химические реакции обычно проводятся в узком интервале температур, то зависимость А от Т так резко не выражается, что приводит к настоящему наклону прямой Аррениуса.
Ответ: n = −2.
4. Гидролиз (CН2)6СС1СН3 в 80 %-м этаноле протекает по первому порядку. В одном из опытов для этой реакции были получены следующие значения константы скорости:
| Т, К | 273 | 298 | 308 | 318 |
| K ,с | 1,06∙10-5 | 3,19∙10-4 | 9,86∙10-4 | 2,92∙10-3 |
Рассчитайте энергию активации и предэкспоненциальный множитель.
Решение. По формуле Аррениуса определяем энергию активации: lgk2/k1 = Eоп(T2-T1)/(2,3.RT1.T2); Еср = 957 кДж/моль. Для нахождения k0 можно взять любую температуру. lgk = lgk0 - -E / RT; lgko = lgk+E . RT . Т = 298К. lgkо= lg(3,19.104) + +957/(2,303 х х 8,314.298) = 13,28. k0= 1,9.1013e-0,5700/RT.
Ответ: k0= 1,9∙1013е-0,5700/RT.
5. Вещество разлагается двумя параллельными путями с константами скорости k1 и k2. Какова разность энергий активации этих двух реакций, если при Т = 283 К k1/k2 = 10, а при Т = 313 К - k1/k2 = 0,1.
Решение. Схема реакции: В А ® С. Введем обозначения: а – начальная концентрация А; х – общее число молей вещества А, превратившегося в продукты В(х1) и С(х2); х = х1 + х2.
Для параллельных реакций k1+k2 = k. Учитывая, что k = = k0∙е-Еоп /RT, получим для Т1=283 К: А ® В, для Т2 = 313К: А ® ® С. По уравнению Аррениуса: lgk2/k1=Eоп.(T2 − T1 )/(2,3.R.T1.T2), откуда Е1 = -56,53 кДж/моль и Е2 = 56,53 кДж/моль.
Отрицательная энергия активации для направления А ® В по сравнению с направлением А ® С в параллельных реакциях говорит о том, что при повышении температуры константа скорости реакции в первом направлении падает. Значит, при повышенных температурах вещество А с большей скоростью превращается не в вещество В, а в вещество С. Одной из реакций подобного типа является образование нитрозилбромида по схеме: 2 NО + Вr ® 2 NОВr.
Дифференциальное кинетическое уравнение этой реакции имеет вид d[NOBr]/dt = К[NO]2[Br2] и согласуется со следующими стадиями процесса:
1) NO+Br2 « NOBr2; 2) NOBr2+NO « 2 NOBr
Опыты показывают, что энергия активации этой реакции отрицательна. Это может быть в том случае, когда при повышенных температурах скорость распада NOBr2 на NO и Br2 с константой скорости k2 концентрация NOBr2 уменьшается, что ведет к уменьшению скорости образования NOBr на второй ста-дии. Следовательно, из-за уменьшения константы скорости на лимитирующей стадии по мере повышения температуры энергия активации реакции оказывается величиной отрицательной. По-добные примеры не единичны. Например,в реакции 2NO + O2 « « 2NO2 константа скорости прямой реакции понижается при повышении температуры. Как правило, понижение константы скорости реакции при росте температуры наблюдается для тех реакций, где имеются конкурирующие реакции.
Ответ: Еа1 = -56,53 кД/моль и Еа2 = 23,04 кДж/моль.
|
из
5.00
|
Обсуждение в статье: Зависимость скорости реакции от температуры |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

