 |
Главная |
РЕАКЦИИ ОБМЕНА В РАСТВОРАХ ЭЛЕКТРОЛИТОВ. ГИДРОЛИЗ
|
из
5.00
|
Общие методические указания.
Домашнее задание. При выполнении заданий необходимо знать:
1) в каких случаях реакции обмена в растворах электролитов протекают необратимо?
2) что такое гидролиз, типы гидролиза солей?
3) как определяется степень гидролиза и от каких факторов она зави-сит?
4) что называется константой гидролиза? Выражение Кг для различных типов солей.
5) Какова кислотность среды в водном растворе соли : Na2S,NaNO3, KCl, AlCl3, NH4Cl, K2HPO4, CuSO4?
6) в каком направлении сместится равновесие реакции гидролиза соли Na2СO3 , если к раствору прибавить кислоту (щелочь)?
Таблица 3
| № | Составьте уравне-ния диссоциации следующих соеди-нений | Напишите молекулярные и ионные уравнения реакций | |
| Обмена | Гидролиза солей | ||
| H2SO4, Zn(OH)2 | AlCl3 + 2NaOH → AgNO3 + KCl → | NaHS, Zn(NO3)2, CrCl3 + Na2CO3 + H2O | |
| CH3COOH, H3PO3 | ZnO + NaOH → BaCl2 + K2SO4 → | NiSO4, SnCl4, K2S | |
| H2S, NaH2PO4 | Cr(OH)3 + KOH → MgCl2 + K2SiO3 → | Na2CO3 , CrCl3, Cr 2(SO4) 3 + Na2S + H2O | |
| Ba(OH)2, H2Se | Cu(NO3)2 + NaOH → K2S + Pb(CH3COO)2 → | NaHCO3, Al2 (SO4) 3, NH4NO2 | |
| Ca(HCO3)2, Cr(OH)3 | NaCrO2 + H2SO4 → SnCl2 + Na3PO4 → | Cr(NO3)3, K2SO3, FeCI3 + K2СO3 + H2O | |
| Al(OH)3, Ni(HS)2 | Al2(SO4)3 + 2KOH → CuCl2 + K2S → | Na2SiO3, Сu(NO3)2, CrCl3 +Na2S+H2O | |
| NaHSO3, H3PO4 | CH3COOH + Na2CO3 → CaI2 + Na3PO4 → | MnSO4, Na2S, Al2 (SO4) 3 + Na2S + H2O | |
| Cr(OH)3, NH4OH | Cr(NO3)3 + 2NaOH → BaBr2 + K2SiO3 →. | Fe2(SO4)3, K3PO4 SbCl3 | |
| Zn(OH)2, H2Te | BeCl2 + KOH(изб) → MnSO4 + Na2S3 → | Bi(NO3)3, Al (NO2)3, NiCl2 | |
| Mg(NO2)2, H3AsO4 | Cr2O3 + KOH → Na2SiO3 + MnSO4 → | MnCl2, NaH2PO4, Fe +NH4Cl +H2O | |
| Na3PO4, Mg(HCO3)2 | Al2(SO4)3 + KOH(изб) → AgNO3 + NaBr → | NaNO2, Al2(SO4)3 Sb(NO3)3 | |
| 1 2 | H3AsO3, Zn(OH)2 | CrCl3 + NaOH(изб) → Hg(NO3)2 + KI → | Na2SiO3, Al2(SO4)3, NiCl2 |
| H2S, Cr(OH)3 | Ca(HCO3)2 + H2SO4 → MnSO4 + Na2S → | Pb(NO3)2, K2SiO3, Al2(SO4)3 | |
| Na2SiO3, Cr(OH)3 | Pb(NO3)2 + CuSO4 → Be(NO3)2 + KOH(изб) → | NiSO4, Na2SO3 CH3COO Na | |
| NH4HCO3, Al(OH)3 | CrCl3 + NaOH(изб) → CaCl2 + Na2SO3 → | K2SiO3, Со SO4, (NH4)2S | |
| H2Se, Ca(HCO3)2 | HNO2 + NH4OH → BaS + K2CO3 → | (NH4)2CO3, CuSO4 , Zn+Na2CO3+H2O | |
| Al(OH)3, Mg(NO2)2 | Mg(OH)2 + H2SO4 → Fe(NO3)3 + Na3PO4 → | Mn(NO3)2, Na2CO3, Bi(NO3)3 | |
| Zn(OH)2, CH3COOH | Fe2O3 + H2SO4 → Na3PO4 + Pb(NO3)2 → | KHCO3, CrCl3. Al+ K3PO4 + H2O | |
| Ni(OH)2, H2SO3 | MnSO4 + NaOH → CuSO4 + Ba(NO3)2 → | Cr2(SO4)3, KNO2, Zn+Na2S+H2O | |
| Cr(OH)3, Na2CO3 | Al2(SO4)3 + NaOH(изб) → CrCl3 + Na3PO4 → | KNO2, NiCl2, Mg + NH4Cl +H2O |
Пример выполнения задания :
Вопрос 1.
Составьте уравнение диссоциации следующих соединений Sn(OH)2, CrCl3:
Н+ + НSnО2 -  Sn(OH)2
Sn(OH)2  SnOH+ + OH-
SnOH+ + OH-
↓↑ ↑↓
Н+ + SnО2 2 - Sn 2+ +OH-
Al2(SO4)3 → 2Al3+ + 3SO4 2-
Вопрос 2.
Напишите молекулярные и ионные уравнения реакций обмена:↓
3KOH + Cr(OH)3 = K3 [Cr(OH)6]
Cr(OH)3 + 3OH- = [Cr(OH)6] 3-
Вопрос 3.
Напишите молекулярные и ионные уравнения реакций гидролиза:
Fe 2(SO4)3 + 2H2O  2FeOHSO4 + H2SO4
2FeOHSO4 + H2SO4
Fe3+ + HOH  FeOH 2+ + H+ , pH < 7
FeOH 2+ + H+ , pH < 7

NH4Cl + H2O  NH4OH + HCl
NH4OH + HCl
Na2S + H2O  NaHS + NaOH –
NaHS + NaOH –

CH3COONH4 + H2O < — > CH3COOH + NH4OH
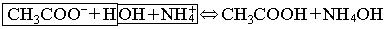
2 AlCl3 + 3Na2CO3 + 3H2O → 2 Al (OH)3 + 3CO 2 + 6NaCl
2 Al3+ + 3CO32– + 3H2O → 2 Al (OH)3 + 3CO 2 .
Задание 5.
|
из
5.00
|
Обсуждение в статье: РЕАКЦИИ ОБМЕНА В РАСТВОРАХ ЭЛЕКТРОЛИТОВ. ГИДРОЛИЗ |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

