 |
Главная |
Идеальный газ во внешнем гравитационном поле
|
из
5.00
|
Пусть ИГ находится во внешнем гравитационном поле (в поле силы тяжести Земли). При нахождении концентрации молекул газа n(x, y, z) в этом поле будем исходить из предположения, что любой бесконечно малый объем газа находится в состоянии механического равновесия, а температура газа T во всех точках одинакова. Только при выполнении этих условий состояние газа можно считать равновесным, так как иначе в газе возникли бы потоки вещества и теплоты, что сделало бы состояние газа неравновесным.
Поле силы тяжести Земли будем считать однородным. Ось OZ направлена вертикально вверх. Тогда концентрация молекул газа будет зависеть только от координаты z (высоты h): n=n(z)или n=n(h). На рис. (1) схематически изображен бесконечно малый выделенный объем газа dV=dSdz, находящийся в равновесии.
 Снизу на этот выделенный объем газа воздействует давление p, а сверху – соответственно давление p+dp. Разность давлений на нижнее и верхнее основание выделенного объема газа dV=dSdz равна гидростатическому давлению:
Снизу на этот выделенный объем газа воздействует давление p, а сверху – соответственно давление p+dp. Разность давлений на нижнее и верхнее основание выделенного объема газа dV=dSdz равна гидростатическому давлению:
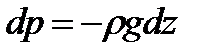 где: r=(Mp)/(RT) – плотность газа, g – ускорение свободного падения, M – молярная масса газа.
где: r=(Mp)/(RT) – плотность газа, g – ускорение свободного падения, M – молярная масса газа.
Отсюда
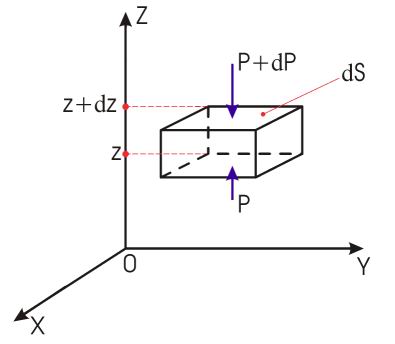
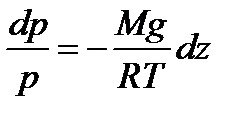
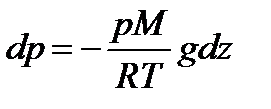 Подставим в полученное выражения плотность газа:
Подставим в полученное выражения плотность газа:
 Из этого уравнения следует, что
Из этого уравнения следует, что
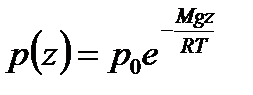 Интегрирование последнего уравнения при условии позволяет определить зависимость давления от высоты:
Интегрирование последнего уравнения при условии позволяет определить зависимость давления от высоты:
 где p0 - давление газа на высоте, принятой за начало отсчета.
где p0 - давление газа на высоте, принятой за начало отсчета.
С учетом формулы для постоянной Больцмана:
и того, что М = m0NA и z = h
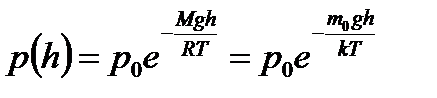 Барометрическая формула:
Барометрическая формула:
Барометрическая формула позволяет рассчитывать зависимость давления атмосферы от высоты в случае, если температура атмосферы постоянна, а гравитационное поле - однородно. Для реальной атмосферы Земли на высотах примерно до 10 км её температура уменьшается в среднем на 6 К на 1 км подъема. Далее до высот порядка 20 км температура остается практически постоянной, а выше - постепенно возрастает до ~ 270 К на высоте около 55 км. На этой высоте давление атмосферы становится уже меньше 0,001 от атмосферного давления на уровне моря.
Несмотря на указанную зависимость температуры атмосферы Земли от высоты, барометрическая формула позволяет достаточно точно определять высоту по результатам измерения давления, что нашло применение в приборах, предназначенных для определения высоты полета самолетов.

Распределение Больцмана было получено в 1866 году Л. Больцманом. Это распределение позволяет рассчитывать концентрацию газа, находящегося в равновесном состоянии во внешнем силовом поле. Причем это поле не должно быть обязательно гравитационным, а может иметь любое происхождение, в частности, быть электростатическим или полем сил инерции.
Анализ распределения Больцмана показывает, что концентрация молекул газа тем выше, чем меньше их потенциальная энергия. Кроме этого, с понижением температуры увеличивается отличие концентраций в точках с различными значениями потенциальной энергии молекул. А при стремлении температуры к абсолютному нулю, молекулы начинают скапливаться в месте, где их потенциальная энергия принимает наименьшее значение. Указанные особенности распределения Больцмана являются следствием теплового движения молекул, так как кинетическая энергия их поступательного движения в среднем равна Wк=(3/2)kT и уменьшается пропорционально уменьшению температуры. А уменьшение кинетической энергии приводит к уменьшению количества молекул, способных преодолеть потенциальный порог, высота которого характеризуется величиной потенциальной энергии высотой Wp.
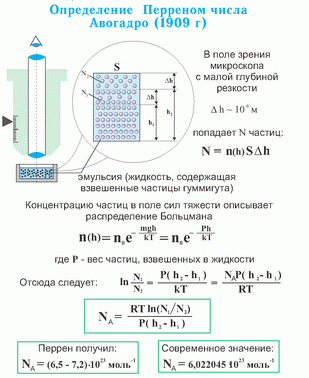
Опыт Перрена.
Распределение Больцмана было использовано французским физиком Жаном Батистом Перреном (1870–1942) при экспериментальном определения постоянной Больцмана k и постоянной Авогадро NA.
 В работах, выполненных Перреном в 1908-1911 гг., измерялось распределение концентрации микроскопических частиц во внешнем гравитационном поле. Отметим, что совокупность микрочастиц, находящихся во взвешенном состоянии в жидкости, близка по своей молекулярно-кинетической структуре к идеальному газу и может описываться газовыми законами. Это дает возможность при определении распределения микрочастиц во внешнем силовом поле использовать формулу Больцмана.
В работах, выполненных Перреном в 1908-1911 гг., измерялось распределение концентрации микроскопических частиц во внешнем гравитационном поле. Отметим, что совокупность микрочастиц, находящихся во взвешенном состоянии в жидкости, близка по своей молекулярно-кинетической структуре к идеальному газу и может описываться газовыми законами. Это дает возможность при определении распределения микрочастиц во внешнем силовом поле использовать формулу Больцмана.
 Исследуя в микроскоп броуновское движение, Ж. Перрен убедился, что броуновские частицы распределяются по высоте подобно молекулам газа в поле тяготения. Применив к этим частицам больцмановское распределение, можно записать:
Исследуя в микроскоп броуновское движение, Ж. Перрен убедился, что броуновские частицы распределяются по высоте подобно молекулам газа в поле тяготения. Применив к этим частицам больцмановское распределение, можно записать:
где m – масса частицы,
m1– масса вытесненной ею жидкости;
m=4/3πr3ρ, m1= 4/3πr3ρ1
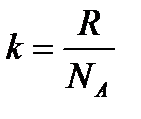 (r – радиус частицы, ρ – плотность частицы, ρ1– плотность жидкости).
(r – радиус частицы, ρ – плотность частицы, ρ1– плотность жидкости).
Если n1 и n2 – концентрации частиц на уровнях h1 и h2,
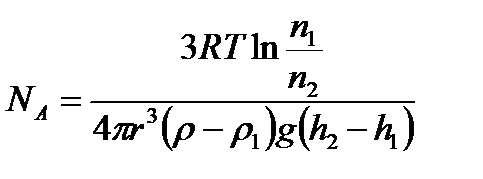
Значение NA, получаемое из работ Ж. Перрена, соответствовало значениям, полученным в других опытах. Это подтверждает применимость к броуновским частицам распределения Больцмана.
|
из
5.00
|
Обсуждение в статье: Идеальный газ во внешнем гравитационном поле |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

