 |
Главная |
ЛАБОРАТОРНЫЕ РАБОТЫ ПО ТЕМЕ
|
из
5.00
|
«РАСТВОРЫ ЭЛЕКТРОЛИТОВ»
Лабораторная работа № 1. Сильные и слабые электролиты
Опыт 1. Окраска индикаторов в различных средах.
В одну пробирку налейте 5-6 капель 2 н. H2SO4, в другую – такой же объем 2 н. NaOH, в третью – такой же объем дистиллированной воды. Во все три пробирки добавьте по 1 капле раствора фенолфталеина. Отметьте цвет раствора в каждой пробирке. Аналогичный опыт проделайте с индикатором метиловым оранжевым. Результаты наблюдений занесите в таблицу:
| Индикатор | Среда | ||
| кислая | нейтральная | щелочная | |
| Фенолфталеин | |||
| Метиловый оранжевый |
Опыт 2.Определение pH растворов кислот
HCl, H2SO4, CH3COOH
На часовое стекло положить полоски универсального индикатора, нанести на них 1-2 капли испытуемого раствора и тотчас же сравнить окраску бумаги со шкалой универсального индикатора. Сделать выводы о силе электролитов. Записать уравнения диссоциации.
Опыт 3.Определение рН растворов оснований
NaOH, Ca(OH)2, NH4OH
На часовое стекло положить полоски универсального индикатора, нанести на них 1-2 капли испытуемого раствора и тотчас же сравнить окраску бумаги со шкалой универсального индикатора. Сделать выводы о силе электролитов. Записать уравнения диссоциации.
Лабораторная работа № 2. Смещение ионного равновесия. Ионные реакции с образованием слабого электролита
Опыт 1. Налейте в две пробирки по 5-6 капель 0,1 н. раствора гидроксида аммония и по 1-2 капли раствора фенолфталеина. Затем в одну из пробирок бросьте 1 кристалл хлорида аммония. Пробирку встряхните несколько раз. Наблюдайте ослабление интенсивности окраски раствора.
Гидроксид аммония – слабый электролит. В его растворе имеет место равновесие: NH4OH ↔ NH4++OH–. Ионы ОН– и обусловливают окраску фенолфталеина. Добавление NH4Cl, который диссоциирует на ионы NH4+ и Cl–, значительно увеличивает концентрацию ионов NH4+ в растворе. А это нарушает равновесие между молекулами NH4OH и ионами NH4+ и OH–, смещая его влево, т.е. ионы NH4+ и OH– соединяются и образуют недиссоциированные молекулы NH4OH. В результате концентрация ионов ОН– в растворе очень сильно понижается и окраска раствора бледнеет.
Опыт 2. Налейте в две пробирки по 5-6 капель 0,1 н. раствора уксусной (CH3COOH) кислоты и по 1-2 капли раствора метилового оранжевого. Затем в одну из пробирок введите 2-3 кристаллика ацетата натрия (CH3COONa). Пробирку встряхните несколько раз. Сравните интенсивность окраски в пробирках. Объясните причину изменения окраски раствора.
Опыт 3.Ионные реакции с образованием слабого электролита
а) Положите в пробирку несколько кристаллов хлорида аммония (NH4Cl) и прилейте раствор гидроксида натрия (NaOH). Определите выделяющийся газ по запаху, слегка нагрев пробирку.
б) Опустите в пробирку несколько кристаллов ацетата натрия (CH3COONa) и прилейте разбавленную серную кислоту. Напишите уравнение реакции.
Лабораторная работа № 3. Произведение растворимости
Опыт 1.Ионные реакции с образованием осадков
а) Налейте в три пробирки по 2-3 капли раствора хлорида бария (BaCl2) и добавьте в одну из них несколько капель раствора сульфата натрия (Na2SO4), в другую – раствора серной кислоты, в третью – раствора сульфата алюминия (Al2(SO4)3). Наблюдайте появление одинакового осадка. Составьте уравнения реакций. Что можно сказать о сущности реакций в проделанном опыте?
б) Налейте в одну пробирку 2-3 капли сульфата железа (FeSO4) (II)? а во вторую – такой же объем раствора сульфата меди (CuSO4) (II). Прилейте в обе пробирки по 3-4 капли раствора сульфида натрия (Na2S). Составьте уравнения реакций. Слейте растворы, а осадки сохраните для следующих опытов.
Опыт 2.Образование осадков и произведение растворимости
В две пробирки налейте по 3-4 капли 0,005 М раствора нитрата свинца (Pb(NO3)2). В одну из них прибавьте такой же объем 0,05 М раствора хлорида калия (KCl), а в другую – такой же объём 0,05 М раствора иодида калия (KI). В какой из пробирок выпал осадок? Объясните полученный результат, используя значения произведений растворимости. Составьте уравнения реакций.
Опыт 3. Растворение осадков и произведение растворимости
К осадкам FeS и CuS, полученным в опыте 1.б). Прилейте немного 2 н. раствора соляной кислоты. Какой из осадков растворился? Составьте уравнение реакции. Объясните различие в растворимости осадков, используя значения произведений растворимости.
ЗАДАНИЯ ДЛЯ САМОСТОЯТЕЛЬНОЙ РАБОТЫ
Слабые электролиты
Примеры решения задач
Задача 1.1. Степень диссоциации уксусной кислоты в 0,1 М растворе равна 1,32∙10–2. Найти константу диссоциации кислоты и значение рК.
Решение. Подставим данные задачи в уравнение закона разбавления Оствальда
К = α2CM/(1–α) = 1,77∙10–5 pK = -lg K = 4,75
Задача 1.2.Вычислить концентрацию ионов водорода в 0,1 М растворе хлорноватистой кислоты HClO (K=5∙10-8).
Решение: Найдем степень диссоциации HClO
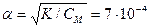 . Отсюда [H+] = α∙CM = 7∙10–5 моль.
. Отсюда [H+] = α∙CM = 7∙10–5 моль.
Задачу можно решить и другим способом, используя соотношение
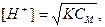 тогда [H+] = 7∙10–5 моль/л.
тогда [H+] = 7∙10–5 моль/л.
Задача 1.3. Во сколько раз уменьшится концентрация ионов водорода в 0,2 М растворе HCOOH (K = 0,8∙10–4), если к 1 л этого раствора добавить 0,1 моль HCOONa? Считать, что соль полностью диссоциирована.
Решение: HCOOH  H+ + НCOO–
H+ + НCOO–
HCOONa → HCOO– + Na+
Исходная концентрация ионов водорода:
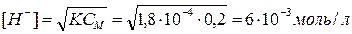 .
.
Концентрацию ионов водорода в растворе после добавления соли обозначим х. Тогда концентрация недиссоциированных молекул кислоты равна (0,2-х). Концентрация же ионов HCOO– слагается из двух величин: из концентрации, создаваемой диссоциацией молекул кислоты, и концентрации, обусловленной присутствием в растворе соли. Общая концентрация ионов HCOO– равна, следовательно, (0,1+х)
 откуда х = 3,6∙10–4 моль/л.
откуда х = 3,6∙10–4 моль/л.
Сравнивая исходную концентрацию ионов водорода с найденной, находим, что прибавление соли HCOONa вызвало уменьшение концентрации ионов [H+] в 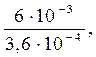 т.е. в 16,6 раза.
т.е. в 16,6 раза.
Задачи для самостоятельной работы:
1.4. Нужно приготовить раствор, содержащий в 1 л 0,5 моля NaCl, 0,16 моля KCl и 0,24 моля K2SO4. Как это сделать, имея в своем распоряжении только NaCl, KCl и Na2SO4?
1.5. Константа диссоциации масляной кислоты C3H7COOH 1,5∙10–5. Вычислить степень её диссоциации в 0,005 М растворе.
1.6. Найти степень диссоциации хлорноватистой кислоты HOCl в 0,2 н. растворе.
1.7. Степень диссоциации муравьиной кислоты HCOOH в 0,2 н. растворе равна 0,03. Определить константу диссоциации кислоты и значение рК.
1.8. Степень диссоциации угольной кислоты H2CO3 по первой ступени в 0,1 н. растворе равна 2,11∙10–3. Вычислить К1.
1.9. При какой концентрации раствора степень диссоциации азотистой кислоты HNO2 будет равна 0,2?
1.10. В 0,1 н. растворе степень диссоциации уксусной кислоты равна 1,32∙10–2. При какой концентрации азотистой кислоты HNO2 ее степень диссоциации будет такой же?
1.11. Сколько воды нужно прибавить к 300 мл 0,2 М раствора уксусной кислоты, чтобы степень диссоциации кислоты удвоилась?
1.12. Чему равна концентрация ионов водорода H+ в водном растворе муравьиной кислоты, если α = 0,03?
1.13. Вычислить [H+] в 0,02 М растворе сернистой кислоты. Диссоциацией кислоты по второй ступени пренебречь.
1.14. Вычислить [H+], [HSe–] и [Se2–] в 0,05 М растворе H2Se.
1.15. Во сколько раз уменьшится концентрация ионов водорода, если к 1 л 0,005 М раствора уксусной кислоты добавить 0,05 моля ацетата натрия?
1.16. Рассчитать концентрацию ионов CH3COO– в растворе, 1 л которого содержит 1 моль CH3COOH и 0,1 моля HCl, считая диссоциацию последнего полной.
Сильные электролиты
Пример решения задач
Задача 2.1. Вычислить ионную силу и активность ионов в растворе, содержащем 0,01 моль/л MgSO4 и 0,01 моль/л MgCl2.
Решение: Ионная сила раствора равна

Коэффициент активности иона Mg2+ (и равный ему коэффициент активности иона SO42–) найдем по формуле
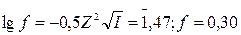
Аналогично находим f для Cl–:
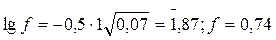
Теперь, пользуясь соотношением а = f∙CM, находим активность каждого иона:

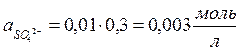

Задачи для самостоятельной работы:
2.2. Вычислить приближенное значение активности ионов K+ и SO42– в 0,01 М растворе K2SO4.
2.3. Вычислить приближенное значение активности ионов Ba2+ и Cl– в 0,002 н. растворе BaCl2.
2.4. Найти приближенное значение коэффициентов активности иона водорода в 0,0005 М растворе H2SO4, содержащем, кроме того, 0,0005 моль/л HCl. Считать, что серная кислота полностью диссоциирует по обеим ступеням.
2.5. Вычислить ионную силу и активность ионов в растворе, содержащем 0,01 моль/л Ca(NO3)2 и 0,01 моль/л CaCl2.
2.6. Вычислить ионную силу и активность ионов в 0,1 %-ном (по массе) растворе BaCl2. Плотность раствора принять равной единице.
2.7. Рассчитать активность иона водорода в 0,005 н. растворе HCl, содержащем, кроме того, 0,15 моль/л NaCl.
2.8. Найти приближенные значения коэффициентов активности ионов Cl–, SO42–, PO43– и [Fe(CN)6]4– в растворе с ионной силой 0,0001.
|
из
5.00
|
Обсуждение в статье: ЛАБОРАТОРНЫЕ РАБОТЫ ПО ТЕМЕ |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

