 |
Главная |
Понятие о комплексных соединениях
|
из
5.00
|
1.Комплексообразователем может быть катион металла побочной подгруппы (Fe+2, Fe+3, Cr+3, Zn+2, Ag+ и др.), многозарядные катионы, например, Al+3 или Si+4.
2. Около катиона-комплексообразователя располагаются (координируются) отрицательно заряженные ионы или нейтральные молекулы – лиганды. Особенность лигандов заключается в том, что атомы неметаллов в анионах или молекулах несут неподеленную пару электронов, которая может участвовать в донорно-акцепторной связи в качестве донора. Комплексообразователь, в свою очередь, имеет несколько свободных орбиталей и может выступать в роли акцептора.
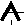
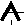
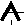
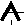
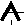
Fe+3 3d 4s –– 4p –– –– ––
При уплотнении электронов (за счет образования спаренных электронов) получаем следующую схему:


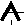
Fe+3 …3d –– –– 4s –– 4p –– –– ––
- Количество лигандов (координационное число) равно числу свободных орбиталей в ионе комплексообразователя. Оно, как правило, численно равно удвоенному заряду комплексообразователя
Заряд комплексообразователя +1 +2 +3 +4
Число лигандов 2 4 (6) 6 (4) 8 (6)
4. Заряд комплексного иона (состав иона записывается в квадратных скобках) рассчитывают алгебраической суммой всех зарядов. Ионы внешней сферы (записываются вне квадратных скобок) компенсируют суммарный заряд комплексного иона.
+2 0 2+ 2-
[Cu(NH3)4] SO4 - сульфат тетрааммин меди (II)
+3 0 3+ -
[Сr(H2O)6] Cl3 - хлорид гексааквохрома (III)
++4 2-
K2 [Pt Cl6] - гексахлороплатинат (IV) калия
+ 3+ - 3-
K3[Fe(CN)6] – гексацианоферрат (III) калия
5. Все комплексные соли, кислоты и основания – растворимые в воде, ярко окрашенные, диссоциируют с образованием комплексного иона и ионов внешней сферы.
[Cu(NH3)] SO4 = [Cu(NH3)] 2+ + SO42-
6. Комплексные соединения применяют в металлургии (извлечение редких металлов), медицине, для умягчения воды, для получения красителей, в качественном анализе (аналитическая химия, криминалистика, археология и т.д.).
Коррозия металлов
Коррозия- самопроизвольный процесс (окислительно-восстановительный) разрушения металлов в результате взаимодействия с окружающей средой.
В зависимости от факторов внешней среды различают химическую (термическую), электрохимическую, биологическую и т.д. коррозии.
Химическая или термическая коррозия протекает в сухом воздухе, в среде неэлектролитов (бензин, сероуглерод и т.п.) при повышенной температуре. Она имеет место при термической обработки металлов, работе двигателей внутреннего сгорания, в отопительных котлах.
4Fe0 + 3O2 =2 Fe2+3O3
сухой
Fe0 + S = Fe+2S
Электрохимическая коррозия наблюдается при взаимодействии металлов с влажной окислительной средой (атмосфера Земли) или с растворами электролитов (например, морская вода).
В нейтральной среде атомы металла окисляются
Fe0 – 2e- = Fe+2
Растворенный в воде кислород восстанавливается
O2 + H2O + 4e- = 4OH-
В качестве продукта реакции образуется гидроксид железа (II)
Fe+2 + 2OH- = Fe(OH)2,
который самопроизвольно окисляется во влажном воздухе до ржавчины
4Fe(OH)2+ 2H2O + O2 = 4Fe(OH)3 или Fe2O3 · nH2O
В кислой среде металл окисляется, а восстанавливается катион водорода.
Zn0 – 2e- = Zn+2
2H+ +2e- = H2↑
Если в металлическом изделии присутствует контакт двух металлов, то окислению подвергается более активный из них. При контакте железо – медь окисляется (с большей скоростью) железо. При контакте железо – алюминий подвергается окислению алюминий.
Способы защиты от коррозии:
- Изменение условий окружающей среды (осушение воздуха, понижение температуры процесса, замена электролитов на неэлектропроводные жидкости и т.д.)
- Покрытие металлов защитными лаками, красками, эмалями, полимерными пленками и т.д.
- Анодная защита (покрытие металлических изделий слоем более активного металла, который будет окисляться, но не даст коррозировать основному изделию).
- Катодная защита (металл покрывают менее активным металлом, который не подвергается коррозии, а тем самым служит защитой для изделия из активного металла). Такого рода защита используется при изготовлении консервных банок.
- Протекторная защита (к основному металлическому изделию прикрепляют небольшие листы или проволоку из более активного металла – протектор; протектор окисляется, обеспечивая сохранность основного изделия). Это метод защиты подземных трубопроводов.
- Замена металлических изделий на полимерные, более устойчивые к воздействию окружающей среды.
|
из
5.00
|
Обсуждение в статье: Понятие о комплексных соединениях |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

