 |
Главная |
Опыт № 2. Качественная реакция на альдегиды.
|
из
5.00
|
В две пробирки налейте по 0,5 см3 фуксинсернистой кислоты. Затем в одну из них добавьте несколько капель формалина, в другую – ацетона. Что наблюдается? Некоторые кетоны вызывают частичное восстановление первоначальной окраски фуксина. Поэтому возникновение слабо-розовой окраски нельзя считать положительной пробой.
Опыт № 3. Образование альдегидов и кетонов гидрогенсульфитных соединений.
В две пробирки налейте по 2 см3 насыщенного раствора гидрогенсульфита натрия NaHSO3, потом в одну пробирку добавьте равный объем ацетона, во вторую – 0,5 см3 бензальдегида. Содержание каждой пробирки перемешайте. Что наблюдается?
Опыт № 4. Взаимодействие бензальдегида со щелочью (реакция Канниццаро-Тищенко).
В пробирке растворите 0,3 см3 бензальдегида в 1 см3 этилового спирта, добавьте 0,5 см3 гидроксида калия с массовой долей КОН 50 % и хорошо перемешайте. Вскоре из раствора выделяется бензоат калия, и масса затвердевает. Для выделения бензилового спирта прогрейте массу, которую получили, с целью выпаривания этилового спирта и растворите бензоат калия, для чего прилейте как можно меньшее количество воды. Бензиловый спирт всплывает в виде масленичного слоя.
Контрольные вопросы:
1. Назовите соединение по международной номенклатуре:
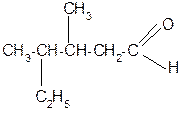 |
а) 3-метил-2-этилпентаналь;
б) 3-метил-4-этилпентаналь;
в) 3,4-диметилгексаналь;
г) 2-этил-3-метилгексанала.
2. С помощью какого из приведенных реактивов можно доказать наличие соединения, содержащего карбонильную группу?
а) раствор гидрогенсульфита натрия;
б) бромная вода;
в) раствор гидроксида натрия;
г) раствор хлорида железа (III).
3. Назовите соединение, которое будет образовываться в результате восстановления бутанона.
а) бутановая кислота
б) бутанол-1;
в) бутанол-2;
г) бутен-2.
4. Приведите структурные формулы изомерных соединений состава С5Н10.
5. Сравните химические свойства гексаналя и гексанона. Приведите схемы соответствующих реакций.
Лабораторная работа № 5
КАРБОНОВЫЕ КИСЛОТЫ
Цель работы: овладение навыками исследования свойств карбоновых кислот; умение студентами самостоятельно наблюдать за преобразованиями реагирующих веществ и делать соответствующие выводы.
Оборудование и реактивы:
– штатив с пробирками;
– горелка;
– водяная баня;
– раствор перманганата калия;
– раствор серной кислоты;
– раствор муравьиной кислоты;
– раствор уксусной кислоты;
– раствор 1 см3 щавелевой кислоты;
– аммиачный раствора оксида серебра (II);
– щавелевая кислота (крист.);
– известковая вода;
– магний (стружка);
– карбонат натрия (крист.);
– водный раствор мыла;
– насыщенный раствор сульфата кальция;
– раствор ацетата свинца (II);
– спиртовой раствор мыла;
– раствор фенолфталеина – индикатор;
– олеиновая кислота;
– бромная вода;
– бензойная кислота;
– 10 %-ый раствор гидроксида натрия;
– раствор бензойной кислоты;
– раствор салициловой кислоты;
– раствор хлорида железа (III).
Опыт № 1. Взаимодействие карбоновых кислот с раствором перманганата калия.
В три пробирки налейте по 3-4 см3 раствора перманганата калия, добавьте по 0,3 см3 разведенной серной кислоты, затем добавьте в одну из них 1 см3 муравьиной кислоты, во вторую – 1 см3 уксусной кислоты, в третью – 1 см3 щавелевой кислоты. В каком случае будет меняться цвет?
Опыт № 2. Восстановительные свойства муравьиной кислоты.
В пробирку налейте 1 см3 аммиачного раствора оксида серебра (II), добавьте 0,5 см3 муравьиной кислоты и нагрейте. Что наблюдается? Сделайте вывод о восстановительных свойствах муравьиной кислоты.
Опыт № 3. Разложение щавелевой кислоты при нагревании.
1 г кристаллической щавелевой кислоты нагрейте в пробирке с газоотводной трубкой, подтянутый конец которой опустить в пробирку с 1 см3 известковой воды. Что наблюдается?
Опыт № 4. Образование солей карбоновых кислот.
а) В пробирку налейте 0,5 см3 уксусной кислоты и добавьте магний в виде стружки. У отверстия пробирки подожгите газ, который выделяется.
б) В пробирку налейте 0,5 см3 разведенной уксусной кислоты и добавьте микрошпатель карбоната натрия. К отверстию пробирки поднесите горящую спичку. Что наблюдается?
Опыт № 5. Свойства высших жирных кислот.
А) образование нерастворимых солей высших жирных кислот.
В три пробирки налейте по 3 см3 водного раствора мыла. В одну из них добавьте водопроводной воды, во вторую – насыщенный раствор сульфата кальция, в третью – раствор ацетата свинца (II). Сравните интенсивность выпадения осадков.
|
из
5.00
|
Обсуждение в статье: Опыт № 2. Качественная реакция на альдегиды. |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

