 |
Главная |
Опыт № 5. Определение реакции жира.
|
из
5.00
|
К слабо щелочному раствору фенолфталеина добавьте немного спиртового раствора жира. Что наблюдается? Добавьте несколько капель раствора щелочи с массовой долей NaОН 10 %. Что наблюдается?
Опыт № 6. Омыление жиров.
Положите в пробирку 0,5 г жира, 2 см3 этилового спирта и 2 см3 раствора гидроксида натрия с массовой долей NaОН 30 %. Перемешивая смесь, нагрейте ее на водяной бане с температурой 80-90 °С в течение 10 минут. К смеси, которую получили, добавьте 15 см3 насыщенного раствора хлорида натрия. Охладите пробирку. Что наблюдается?
Опыт № 7. Определение ненасыщенности жира.
В одну пробирку налейте 3 см3 бромной воды, во вторую – 3 см3 раствора перманганата калия. Затем в каждую из них добавьте по 0,5 см3 растительного масла и энергично размешайте. Как меняется цвет растворов?
Опыт № 8. Образование акролеина при разложении жира.
В сухую пробирку поместите 0,5 г борной кислоты и каплю растительного масла. При слабом нагреве перемешайте содержимое, затем нагрейте сильнее. Обратите внимание на запах.
Контрольные вопросы:
1. Какая из приведенных соединений относится к классу сложных эфиров?
а) диэтиловый эфир;
б) ацетилсалициловая кислота;
в) этилпропиловый эфир;
г) уксусный ангидрид.
2.
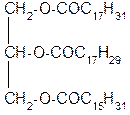 |
Назовите триглицерид:
а) дистеаропальмитат;
б) линолеолиноленопальмитат;
в) олеолинолеостеарат;
г) диолеопальмитат.
3. Какие продукты образуются в результате реакции гидролиза бутилформиата?
а) метанол и бутанол;
б) формальдегид и бутиловый спирт;
в) метанол и масляная кислота;
г) бутанол и муравьиная кислота.
4. Приведите формулу триглицерида пальмитоолеостеарата.
5. С помощью каких реакций можно доказать содержание в составе жира ненасыщенных высших карбоновых кислот? Приведите схемы этих реакций на примере триглицерида триолеата.
СМЫСЛОВОЙ МОДУЛЬ 3
УГЛЕВОДЫ
Лабораторная работа № 7
УГЛЕВОДЫ (моно-, ди- и полисахариды)
Цель работы: овладение навыками исследования строения и свойств моно-, ди- и полисахаридов; умение студентами самостоятельно наблюдать за преобразованиями реагирующих веществ и делать соответствующие выводы.
Оборудование и реактивы:
– штатив с пробирками;
– горелка;
– водяная баня;
– штатив;
– металлическая сетка;
– термостойкая колба;
– D-глюкоза;
– мальтозы;
– лактоза;
– сахароза;
– 5 %-ый раствор сульфата меди (II);
– аммиачный раствор оксида серебра (II);
– реактив Фелинга (7%-ный раствор сульфата меди и 34,6 %-ный раствор сегнетовой соли в 10 %-ном растворе гидроксида натрия);
– реактив Селиванова (0,05 г резорцина растворяют в 100 мл 20 %-ной соляной кислоты);
– йодная вода (раствор йода в йодиде калия);
– раствор перманганата калия;
– 20 %-ый раствор серной кислоты;
– 10 %-ый раствор гидроксида натрия.
Опыт № 1. Доказательство наличия гидроксильных групп в D-глюкозе и дисахаридах.
В пробирки налейте по 1 см3 растворов D-глюкозы, мальтозы, лактозы и сахарозы, добавьте по 2 см3 раствора гидроксида натрия с массовой долей NаОН 10 %. Затем добавьте по 0,5 см3 раствора сульфата меди (II) с массовой долей СuSО4 5 %. Осадок гидроксида меди (II), который образовался, быстро растворяется, и в пробирках образуются прозрачные растворы синего цвета. Эти растворы храните для последующего опыта.
Опыт № 2. Восстановительное действие углеводов.
Растворы, которые получили в предыдущем опыте, нагрейте до кипения. Что наблюдается? Сделайте вывод о восстановительном действии D-глюкозы, мальтозы, лактозы и сахарозы по отношению к соли медь (II).
Опыт № 3. Реакция «серебряного зеркала» (реакция Толленса).
Налейте в пробирку 1 см3 аммиачные раствора оксида серебра (II), добавьте 1 см3 раствора глюкозы и одну каплю раствора гидроксида натрия. Смесь немного нагрейте. Что наблюдается?
Опыт № 4. Взаимодействие углеводов с реактивом Фелинга.
Смешайте в пробирке 0,5 см3 реактива Фелинга и 0,5 см3 раствора глюкозы. Смесь нагрейте до кипения. Такой же опыт сделайте с раствором мальтозы, лактозы, сахарозы. Что наблюдается?
Опыт № 5. Гидролиз сахарозы.
Налейте в пробирку 4-5 см3 раствора сахарозы и добавьте 0,5 см3 разведенной серной кислоты. Пробирку нагрейте на водяной бане 10-15 минут. Раствор разделите на две пробирки. В одной пробирке нейтрализуйте содержание раствором гидроксида натрия, а затем добавьте 0,5 см3 реактива Фелинга и нагрейте на водяной бане Во вторую пробирку добавьте несколько капель реактива Селиванова и нагрейте на водяной бане. Что наблюдается?
|
из
5.00
|
Обсуждение в статье: Опыт № 5. Определение реакции жира. |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

