 |
Главная |
Описание математической модели процесса окисления сульфидного цинкового концентрата в кипящем слое
|
из
5.00
|
В [5] разработана математическая модель периодического процесса окисления сульфидного цинкового концентрата в кипящем слое, в основу которой положена гипотеза о механизме процесса, составленная на основании сведений литературы. Результаты исследования процесса окислительного обжига математическим моделированием изложены в [5], где показано, что скорости окисления сульфидов цинка и железа одинаковы и процесс окисления в частице концентрата протекает зонально. Эти результаты позволяют процесс окисления цинкового концентрата в сете поставленной в [5] цели представить как
2MeS+3O2 =2MeO+2SO2 (1)
где Me - цинк, MeS - сульфидная фаза, MeO - оксидная фаза.
Такое представление о процессе позволяет при принятых в [5] допущениях несколько упростить математическую модель [5]. Действительно, зная текущие массы сульфидной и оксидной фазы и содержание компонентов в частице концентрата, можно определить содержание последних в частице огарка в любой момент окисления.
Изменение во времени текущей массы сульфидной фазы может быть описано уравнением Валенсии [7], выведенным для реакций, аналогичных реакции (1):
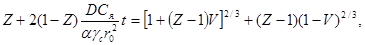 (2)
(2)
где

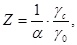

где Gc (0) - первоначальная масса частицы концентрата, г; Gc ( t) - текущая масса сульфидов, т.е. масса неокисленного сульфидного ядра частицы, г; γc - плотность сульфидной фазы, г/см3; γ0 - плотность оксидной фазы, г/см3; α-коэффициент пропорциональности, подобный стехиометрическому (численно равен массе оксидной фазы, образующейся при взаимодействии по (1) единицы массы кислорода); r0 - первоначальный радиус частицы концентрата, см; Cя - концентрация кислорода в ядре потока, об. %; t - текущее время, мин; D - коэффициент диффузии кислорода через слой оксидной фазы, г/ (см. %. мин).
Текущая масса оксидной фазы будет
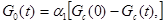 (3)
(3)
где α1 - коэффициент пропорциональности, подобный стехиометрическому, определяется по содержанию компонентов в концентрате и стехиометрическим коэффициентам соответствующих химических реакций и может быть уточнен по результатам анализов огарков, получаемых при обжиге концентрата, например, на лабораторной установке кипящего слоя.
Текущие массы цинка и железа, связанных в сульфид, и сульфидной серы в окисляющейся частице концентрата описываются следующимим выражениями:
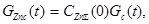 (4),
(4),  (5)
(5)
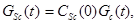 (6)
(6)
где CZn S (0), CFe S (0), CS c (0) - содержания цинка, железа и серы в концентрате. Текущие массы цинка и железа, образующихся в результате окисления сульфидов и находящиеся в частице в оксидной форме, выразим как
 (7),
(7),  (8)
(8)
На основании результатов исследования процесса [5] считаем, что масса гематита в частице огарка меняется во времени пропорционально изменению массы оксидной фазы, а образование феррита цинка происходит со скоростью, превосходящей скорость образования оксида железа. Тогда текущую массу цинка, связанного в феррит, опишем выражением
 (9)
(9)
где D1 - стехиометрический коэффициент.
Потери цинка испарением опишем уравнением, преобразованным к виду, удобному для решения на ЭВМ,
 (10)
(10)
где Ки - коэффициент массопередачи, a - коэффициент линеаризации (при t£15 мин GZn исп (t) =0). Текущая масса кислоторастворимых соединений цинка в частице огарка будет равна
 (11)
(11)
Текущая масса цинка общего в частице
 (12)
(12)
Текущая масса частицы огарка
 (13)
(13)
Уравнение (13) справедливо, если плотности оксидной и сульфидной фаз определены экспериментально для конкретного вида концентрата и полученного из него огарка. Если же плотности определены расчетом с использованием справочных данных, то в (13) необходимо включить член, учитывающий массу "инертных" веществ, например, диоксида кремния и др.
Содержание цинка общего, кислоторастворимого, сульфидного и ферритного рассчитываем по формулам:
 (14)
(14)
 (15)
(15)
 (16)
(16)
 (17)
(17)
а содержание сульфидной серы
 (18)
(18)
Таким образом, математическую модель периодического процесса окисления сульфидного цинкового концентрата в кипящем слое в виде, удобном для решения с помощью ЭВМ, может быть представлена системой уравнений (2) - (18).
Другой моделью, позволяющей решать задачи оптимизации режимов обжига цинковых концентратов в печах кипящего слоя является математическую модель процесса, которая, в частности, описывала бы зависимости содержания кислоторастворимого (Znкр), связанного в феррит (Znф) и сульфид (Znс) цинка в огарке от температуры, состава и размера частиц концентрата и концентрации кислорода в газе. Приведенные математические модели не отвечают этому требованию. На первом этапе составления требуемой модели следует составить систему уравнений, описывающих динамику окисления сфалерита. С этой целью разработана гипотеза о механизме процесса, согласно которой в развитом периоде процесса кислород из ядра газового потока диффундирует через ламинарную газовую пленку к внешней поверхности частицы и адсорбируется на ней, а затем через слой ранее образованных оксидов (толщиной l) двигается к реакционной поверхности (площадью S). В результате электронного обмена на реакционной поверхности протекают реакции окисления сульфидов. Между образующимися оксидами цинка и железа протекает реакция образования феррита цинка. Продукты окисления частицы концентрата определяется скоростью внутренней диффузии [8-10].
При составлении математической модели были приняты следующие допущения:
1. частица концентрата состоит из сульфидов цинка и железа и инертных по отношению к цинку веществ;
2. частицы концентрата имеют форму шара одинакового радиуса;
3. начальные этапы окисления, протекающие не по внутридиффузионному механизму, заканчиваются быстро и вносят относительно малый вклад в общую степень окисления;
4. все точки реакционной поверхности равнодоступны для диффундиру-ющих веществ;
5. частицы концентрата в процесс окисления незначительно изменяют свои размеры.
Скорость образования оксидов цинка и железа определяется скоростью диффузии кислорода к реакционной поверхности, т.е.
 (19)
(19)
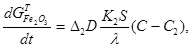 (20)
(20)
при t=0  и
и 
где 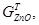
 - текущие массы оксидов, г; D - здесь и далее стехиометрические коэффициенты пересчета; D - коэффициент диффузии в слое оксидов, г/ (с см. %); К1, К2 - доли поверхности S, занимаемые сульфидами цинка и железа; С - концентрация кислорода в ядре потока газа, об. %; С1, С2 - равновесные концентрации кислорода в системах Zn-S-O2 и Fe-S-O2.
- текущие массы оксидов, г; D - здесь и далее стехиометрические коэффициенты пересчета; D - коэффициент диффузии в слое оксидов, г/ (с см. %); К1, К2 - доли поверхности S, занимаемые сульфидами цинка и железа; С - концентрация кислорода в ядре потока газа, об. %; С1, С2 - равновесные концентрации кислорода в системах Zn-S-O2 и Fe-S-O2.
Образующийся оксид железа, взаимодействуя с оксидом цинка, образует феррит цинка
 (21), при t=0,
(21), при t=0, 
 (22)
(22)
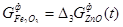 , (23)
, (23)
где  - масса оксида цинка, связанная в феррит в момент времени t, Кф - макроконстанта скорости реакции, 1/с;
- масса оксида цинка, связанная в феррит в момент времени t, Кф - макроконстанта скорости реакции, 1/с; 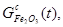
 - текущие массы свободного оксида железа и связанного в феррит, г; М - доля оксида железа, вступающего в реакцию.
- текущие массы свободного оксида железа и связанного в феррит, г; М - доля оксида железа, вступающего в реакцию.
Уравнения материального баланса:
1) текущая масса свободного оксида цинка в частице огарка
 (24)
(24)
2) текущие массы сульфидов цинка и железа
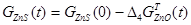
при t=0  (25)
(25)

при t=0 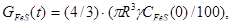 (26)
(26)
где GZnS (0), GFeS (0) - начальные массы сульфидов в частице концентрата; R - радиус частицы концентрата; g - плотность концентрата; С ZnS (0), С FeS (0) - содержание сульфидов цинка и железа в концентрате, масс. %;
3) текущая масса окисляющейся частицы концентрата
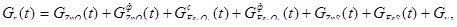 (27)
(27)
где Gи - масса инертных веществ.
Влияние температуры на процесс окисления и ферритообразования выражается в соответствии с законом Аррениуса:
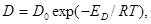 (28)
(28)
 (29)
(29)
Площадь реакционной поверхности и толщина слоя оксидов определяется через текущие массы твердых веществ. При этом введены поправочные коэффициенты a и b, которые учитывают отклонение формы реальных частиц концентрата от идеальных по гладкости и шарообразности, а также разницу между вычисляемыми величинами площади и толщины и реальными, обусловленную присутствием в зернах концентрата посторонних (инертных) примесей:
 (30)
(30)
 (31)
(31)
где gi - плотность соответствующих веществ.
Таким образом, периодический процесс окисления сульфидного цинкового концентрата в рамках принятых допущений описывается системой уравнений (1) - (13).
Параметрическая идентификация математической модели осуществляется по экспериментальным данным, при этом определяли содержание цинка в огарках обжига. Поэтому в систему (19) и (31) введено уравнение
 (32)
(32)
Расчеты показали, что в условиях эксперимента C1»10-15 и С2»10-54, поэтому принимаем С1=С2=0.
В качестве критерия идентификации использовано выражение
 (33)
(33)
где 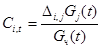 - содержание i-го вещества в (t) - ый момент времени, полученное решением системы уравнений (19) - (32);
- содержание i-го вещества в (t) - ый момент времени, полученное решением системы уравнений (19) - (32);  - получено экспериментально:
- получено экспериментально:
i - ZnS; Znкр; Znc; Znф; i=1; 2; 3; 4; j - ZnS; ZnO; Znc; ZnO Fe2O3
(t) - 0; 1; 2; 5; 10; 20; 40; 60 мин, t=1; 2; 3; …; 8.
Цель идентификации - отыскание численных значений D K1 a/ b и KфM при выполнении условий (33).
В процессе идентификации выяснилось, что  изменяется во времени строго в соответствии с изменением
изменяется во времени строго в соответствии с изменением  . Поэтому с целью упрощения модели уравнение (20) было заменено на
. Поэтому с целью упрощения модели уравнение (20) было заменено на
 (34) при этом
(34) при этом
 (35)
(35)
где  и
и 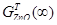 - массы Fe2O3 и ZnO, которые образуются при полном окислении сульфидов железа и цинка, находившихся в порции концентрата (в частице).
- массы Fe2O3 и ZnO, которые образуются при полном окислении сульфидов железа и цинка, находившихся в порции концентрата (в частице).
Результаты решения системы (19) - (32) оказались полностью идентичными результатам решений, полученным после замены (20) на (34).
Таким образом, получена математическая модель [5] процесса окисления сульфидного цинкового концентрата, позволяющая исследовать влияние температуры, состава и размера частиц концентрата и концентрации кислорода на содержание в огарке кислоторастворимого и связанного в феррит и сульфид цинка.
|
из
5.00
|
Обсуждение в статье: Описание математической модели процесса окисления сульфидного цинкового концентрата в кипящем слое |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

