 |
Главная |
Определение ионов, не обладающих окислительно-восстановительными свойствами
|
из
5.00
|
В данных анализах применяют титрование по способу замещения.
Этим способом могут быть определены: Ca2+, Sr2+, Ba2+, Pb2+, Zn2+ и др., которые образуют малорастворимые оксалаты.
Например, при определении кальция ионы Са2+ осаждают оксалатом аммония
Ca2+ + C2O42- = CaC2O4 ¯
Осадок CaC2O4 отфильтровывают, промывают, растворяют в H2SO4 и выделившуюся H2C2O4 титруют стандартным раствором KMnO4.
Пример. Определение СаO в известняке.
Навеска известняка 0,1700 г растворена и обработана избытком оксалата аммония. Осадок отфильтрован, промыт и растворен в H2SO4. Полученный раствор оттитрован 31,50 мл раствора KMnO4.
Т (KMnO4) = 0,002980 г/мл
Определить процентное содержание СаО в известняке.
Химическая сущность
CaCO3 + 2CH3COOH = Ca(CH3COO)2 + H2CO3
Ca(CH3COO)2 + (NH4)2C2O4 = CaC2O4 ¯ + 2CH3COONH4
CaC2O4 + H2SO4 ® CaSO4 + H2C2O4
Количество выделившейся H2C2O4 эквивалентно содержанию СаO в известняке.
5H2C2O4 + 2KMnO4 + 3H2SO4 = 2MnSO4 + 10СO2 + K2SO4 + 8H2O
| MnO4- + 8H+ + 5e- ® Mn2+ + 4H2O | |
| H2C2O4 - 2e- ® 2СO2 + 2H+ | |
| 2MnO4- + 5H2C2O4 + 6H+ = 2Mn2+ + 10СО2 + 8H2O |
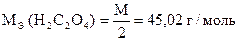
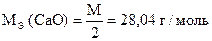
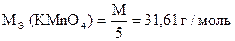
| Дано: |
| m н = 0,1700 г V (KMnO4) = 31,50 мл Т (KMnO4) = 0,002980 г/мл |
| w (СаО) = ? |

‚ ƒ „ …
1) Сколько моль-экв KMnO4 содержится в 1 мл раствора.
2) Сколько моль-экв KMnO4 содержится в 31,50 мл раствора.
Cтолько же моль-экв СаО содержится в навеске.
3) Сколько г СаО содержится в навеске.
4) Сколько г СаО содержится в 1 г образца.
5) Сколько г СаО содержится в 100 г образца или w (СаО).
Опорный конспект по перманганатометрическому методу анализа
Метод перманганатометрии основан на реакциях окисления-восстановления перманганатом калия в кислой среде.
|
|
j 0 MnO4-/ Mn2+ = + 1,51 B
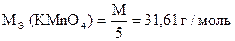
Стандартный раствор - KMnO4
Раствор KMnO4 готовят приблизительной концентрации (установленный) и через 7-10 дней устанавливают точную концентрацию KMnO4 по стандартным веществам:
х.ч. Na2C2O4 ; х.ч. (NH4)2C2O4×H2O ; х.ч. H2C2O4×2H2O.
Методом перманганатометрии анализируют:
1) восстановители - способом прямого титрования
H2C2O4×2H2O, Na2C2O4, (NH4)2C2O4×H2O, H2O2, FeSO4×7H2O, FeO, (NH4)2Fe(SO4)2×6H2O и др.
2) окислители - способом обратного титрования
K2Cr2O7, MnO2, KMnO4, KClO3 и др.
3) вещества, не обладающие окислительно-восстановительными свойствами - способом замещения
CaCO3, Sr(NO3)2, BaCl2, Pb(NO3)2, ZnSO4 и др.
Восстановители, которые разлагаются в кислой среде, титруют реверсивным титрованием (NaNO2, KNO2, Na2SO3, K2SO3 и др).
|
 Fe3+ Fe2+
Fe3+ Fe2+
анализируют способом прямого титрования.
Условия титрования
В качестве среды используют 2н раствор H2SO4 .
HNO3 использовать нельзя, т.к. она является окислителем и до прибавления KMnO4 будет окислять анализируемый восстановитель.
HCl использовать нельзя, т.к. Cl- могут окисляться KMnO4 до Cl2.
CH3COOH использовать нельзя, т.к. кислота слабая, концентрация Н+ мала.
|
из
5.00
|
Обсуждение в статье: Определение ионов, не обладающих окислительно-восстановительными свойствами |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

