 |
Главная |
Проверка домашнего задания. Обобщение и систематизация полученных знаний
|
из
5.00
|
Обобщение и систематизация полученных знаний
Выставление оценок
Домашняя работа: Подготовить доклад на тему: Основные приемы, используемые в физико-химических методах анализа.
СРСП № 25
На тему:Фотоколориметрический метод анализа
Цель:
Обучающая– глубокое изучение различных явлений и законов по данной теме
Развивающая – формирование эффективных и устойчивых взаимосвязей между научной и образовательной деятельностью;
Воспитательная – приобщать обучающихся к активности, самостоятельности на занятиях
Ход урока:
1. Организационный этап- 3 минуты
2. Этап подготовки к усвоению материала СРСП -5 минут
3. Проверка домашнего задания- 27 минут
4. Обобщение и систематизация полученныхзнаний - 5 минут
5. Выставление оценок- 5 минут
В основе метода фотоколориметрии лежит основной закон светопоглощения Ламберта-Бугера-Бера:
А = e×с×  , где:
, где:
А – светопоглощение;
e - молярный коэффициент светопоглощения;
с - молярная концентрация окрашенного вещества в растворе;
l - толщина слоя раствора, см;
Светопоглощение анализируемого раствора прямо пропорциональна концентрации окрашенного раствора и толщине слоя раствора.
Из основного закона фотометрии следует, что основными параметрами фотометрического определения является длина волны, при которой производится измерение А, толщина кюветы и концентрация окрашенного раствора. Сюда же следует отнести и различные химические факторы, связанные с полнотой и условиями фотометрической реакции, концентрацией окрашенных и других реактивов, их устойчивостью и др. В зависимости от свойств анализируемой системы и характеристик применяемого фотометрического прибора выбирают те или иные условия анализа.
Пример: Молярный коэффициент светопоглощения дитизоната меди (II) в тетрахлориде углерода при l = 550нм равен e = 4520; относительная оптическая плотность А = 0,5; длина кюветы равна 5см. Рассчитайте концентрацию меди в растворе.
Решение:
Согласно закону фотометрии А = e×с×  , концентрация меди будет равна:
, концентрация меди будет равна:
с( Cu2+ ) = 0,5/4520×5 = 0,2×10-4 моль/л;
В таблице 14 представлены задания для нахождения с(х) в анализируемом растворе. Задания выполняются самостоятельно, используя:
а) метод градуировочного графика
б) используя основной закон фотометрии Ламберта-Бугера-Бера;
Таблица 14
Рассчитать концентрацию металла в анализируемом растворе используя:
а) прием градуировочного графика, б) по экспериментальным данным колориметрического определения:
| № | Меn+ | с (ст.р-ра) моль/л | А | А(х) | 1, см длина кюветы | Приблиз-ая область длины волны (l, нм) | el | Окраска исслед-го р-ра |
| Fe3+ | 0,2×10-4 | 0,11 | 0,45 | 2,0 | кроваво- | |||
| 0,4×10-4 | 0,22 | красная | ||||||
| 0,6×10-4 | 0,50 | |||||||
| 0,8×10-4 | 0,60 | |||||||
| Zn2+ | 1,0×10-5 | 0,10 | 0,40 | 2,0 | желтая | |||
| 2,0×10-5 | 0,19 | |||||||
| 3,0×10-5 | 0,32 | |||||||
| 4,0×10-5 | 0,5 | |||||||
| Мn2+ | 0,4×10-3 | 0,3 | 0,38 | 3,0 | малино-фиолетовая | |||
| 0,6×10-3 | 0,45 | |||||||
| 0,8×10-3 | 0,6 | |||||||
| 0,9×10-3 | 0,7 | |||||||
| Сu2+ | 0,5×10-3 | 0,15 | 0,75 | 3,0 | синяя | |||
| 1,0×10-3 | 0,30 | |||||||
| 1,5×10-3 | 0.45 | |||||||
| 2,0×10-3 | 0,60 | |||||||
| Со2+ | 0,35×10-3 | 0,45 | 0,56 | 3,5 | синяя | |||
| 0,55×10-3 | 0,69 | |||||||
| 0,65×10-3 | 0,82 | |||||||
| 0,75×10-3 | 0,93 | |||||||
| Ni2 | 0,5×10-4 | 0,12 | 0,45 | 4,0 | красная | |||
| 1,0×10-4 | 0,23 | |||||||
| 2,0×10-4 | 0,46 | |||||||
| 4,0×10-4 | 0,93 | |||||||
| Cr3+ | 0,2×10-4 | 0,23 | 0,55 | 3,0 | оранжевая | |||
| 0,4×10-4 | 0,47 | |||||||
| 0,6×10-4 | 0,69 | |||||||
| 0,8×10-4 | 0,92 |
Проверка домашнего задания
Обобщение и систематизация полученных знаний
Выставление оценок
Домашняя работа: Подготовить доклад на тему: Повышение чувствительности и точности определения веществ высокой чистоты, следов примесей.
СРСП № 26
На тему:Хроматография
Цель:
Обучающая– глубокое изучение различных явлений и законов по данной теме
Развивающая – формирование эффективных и устойчивых взаимосвязей между научной и образовательной деятельностью;
Воспитательная – приобщать обучающихся к активности, самостоятельности на занятиях
Ход урока:
1. Организационный этап- 3 минуты
2. Этап подготовки к усвоению материала СРСП -5 минут
3. Проверка домашнего задания- 27 минут
4. Обобщение и систематизация полученныхзнаний - 5 минут
5. Выставление оценок- 5 минут
Хроматография – универсальный и эффективный физико-химический метод разделения смесей соединений. Используется для решения следующих основных задач:
1. разделение сложных систем различного органического и неорганического происхождения на составные компоненты (например, выделение растительных и животных пигментов);
2. концентрирование веществ из сильно разбавленных растворов (например. микроэлементов из морской воды, почв, горных пород и т.д.);
3. очистка от примесей веществ, таких как витамины, антибиотики.
Вещества при хроматографировании не изменяются химически, что важно при многих исследованиях и проведении анализа. Современные хроматографические методы позволяют не только разделить вещества, но и обнаружить их, идентифицировать и определять.
Любой хроматографический метод основан на распределении вещества между двумя фазами, из которых одна неподвижна (стационарная), другая перемещается относительно первой (подвижная). Компоненты смеси вместе с подвижной фазой переходят через неподвижную и, благодаря различию в относительных скоростях перемещения, разделяются. Разделение веществ связано с сорбционно-десорбционными процессами и возможно в том случае, если стационарная фаза – сорбент – обладает различной сорбционной способностью по отношению к каждому из разделяемых компонентов. При этом под сорбцией понимают любой процесс, связанный с накоплением того или иного компонента в неподвижной фазе или на границе раздела фаз. Таким образом, различие в поведении отдельных компонентов заключается в том, что они перемещаются с неодинаковой скоростью и, соответственно, за один и тот же промежуток времени проходят различные отрезки пути, т.е. имеют разное время удерживания.
Хроматографические методы классифицируют по различным признакам: природе фаз, механизму разделения, технике выполнения и т.д.
Неподвижной фазой может быть твердое вещество, жидкость, нанесенная на твердый носитель или гель. Подвижной фазой – жидкость или газ. По агрегатному состоянию подвижной фазы хроматография подразделяется на жидкостную и газовую. В зависимости от природы твердой фазы различают газо – твердофазную и газо – жидкостную хроматографию, а также жидкостно – твердофазную и жидкостно – жидкостную.
По механизму процесса разделения различают адсорбционную, распределительную, ионообменную, ионную, осадочную и гель-фильтрационную хроматографию.
Хроматографические методы с жидкой подвижной фазой на практике различают по технике выполнения, в зависимости от того, помещена неподвижная фаза в колонку (колоночная хроматография), нанесена в виде слоя на пластинку (тонкослойная хроматография) или распределена в виде пленки на бумаге (бумажная хроматография).
Растворитель, проходящий через колонку, называется элюентом, процесс перемещения вещества вместе с элюентом – элюированием. В результате образуются отдельные хроматографические зоны компонентов смеси, т.е. хроматограмма.
Рассмотрим более подробно несколько видов хроматографии, имеющие наибольшее значение в анализе пищевой, химической и нефтехимической промышленности.
Ионообменная и ионная хроматография. Методы ионообменной хроматографии используется преимущественно для разделения ионов. Количественные определения компонентов после разделения могут быть выполнены любым подходящим методом. Простейшая методика ионообменного разделения состоит в поглощении компонентов смеси ионитов и последовательном элюировании каждого компонента подходящим растворителем. Например, катионы щелочных металлов легко элюируются разбавленным раствором хлороводородной кислоты
(0,1 М HCl). Элюирование раствором 0,1 М HCl позволяет легко разделить Na+ и K+.
Ионообменные методы применяют для определения суммарного содержания катионов или анионов в растворе и для анализа растворов чистых солей. При пропускании через катионит в Н+ - форме раствора, например, соли натрия в результате ионообменного процесса в растворе появляется эквивалентное количество Н+ - ионов:
HR + Na+ = NaR + H+ (1)
Концентрация ионов Н+ в этом растворе может быть определена, например, титрованием и, таким образом, найдена концентрация Na+ в исходном растворе.
Ионная хроматография является одним из вариантов разделения на ионитах, характеризующаяся более высокоэффективной техникой, чем обычная ионообменная хроматография. В этом методе используется поверхностно – слойные сорбенты с небольшой емкостью (10-2 – 10-1 ммоль экв/г) и наибольшим размером частиц (5-50мнм), повышенные давление на входе колонку (2-5 МПа) и высококачественные детектора с автоматической записью сигнала. Для ионной хроматографии характерны экспрестность, удобство работы и более высокая разделительная способность.
Методами ионной хроматогрфии определяют очень многие анионы в питьевой и технической воде, в продуктах технологической переработки в пищевой, фармацевтической и других отраслях промышленности. Известны методики определения галогенидов, нитрата, нитрита, сульфата, ацетата и т.д., всего свыше 70 анионов неорганических и органических кислот. Число катионов значительно меньше. Методами ионной хроматографии определяют главным образом катионы щелочных и щелочно-земельных металлов, а также органические катионы замещенных солей аммония. Определение многих других катионов оказывается ненадежным, т.к. они выпадают в осадок в компенсационной колонке с сильноосновной смолой.
Тонкослойная и бумажная хроматографии. В методе тонкослойной хроматографии (ТСХ) неподвижная твердая фаза тонким слоем наносится на стеклянную, металлическую или пластмассовую пластинку. В 2-3 см от края пластинки на стартовую линию вносят пробу анализируемой жидкости и край пластинки погружают в растворитель, который действует как подвижная фаза жидкостной адсорбционной хроматографии. Под действием капиллярных сил растворитель движется вдоль слоя сорбента и с разной скоростью переносит компоненты смеси, что приводит к их пространственному разделению. Диффузия в тонком слое происходит в продольном и поперечном направлениях, поэтому процесс следует рассматривать как двухмерный. Сорбционные свойства системы в ТСХ характеризуются подвижностью Rf, которая рассчитывается из экспериментальных данных по уравнению:
 (2)
(2)
где: х1 – расстояние от стартовой линии до центра зоны;
хf – расстояние, пройденное за это же время растворителем.
На практике часто пользуются относительной величиной:
 (3)
(3)
где: Rf, ст – также рассчитывается по уравнению (2).
Стандартное вещество (свидетель) в том же растворителе наносится на стартовую линию рядом с анализируемой пробой и, таким образом, хроматографируется в тех же условиях.
Количественные определения в ТСХ могут быть сделаны или непосредственно на пластинке, или после удаления вещества с пластинки. При непосредственном определении на пластинке измеряют тем или иным методом площадь пятна (например, с помощью миллиметровой кальки) и по заранее построенному градуировочному графику находят количество вещества.
Применяют также прямое спектрофотометрирование пластинки с помощью спектроденситометров. Для количественных расчетов также предварительно строят градуировочный график, используя оптическую плотность в центре пятна.
Наиболее точным считается метод, в котором вещество после разделения удаляется с пластинки и анализируется спектрофотометрическим или иным методом. Удаление вещества с пластинки обычно производят механическим путем, хотя иногда применяют вымывание подходящим растворителем.
В настоящее время ТСХ является одним из важных методов аналитической химии. Это непревзойденный метод анализа сложных смесей: он прост по методике выполнения и аппаратуре, экспресен, не требует для анализа больших количеств веществ.
Бумажная хроматография во многом схожа с хроматографией в тонком слое (ТСХ). Важной характеристикой в бумажной распределительной хроматографии, так же как и в ТСХ, является Rf = x/xf, где х – смещение зоны компонента, xf – смещение фронта растворителя. Методика определения Rf в бумажной хроматографии не отличается от соответствующей методики в ТСХ.
По технике выполнения различают следующие виды бумажной хроматографии: одномерную, двухмерную, круговую и электрофоретическую.
Качественный состав пробы в методе бумажной распределительной хроматографии так же, как и в ТСХ, может быть установлен или по специфической окраске отдельных пятен на хроматограмме, или по числовому значению Rf каждого компонента. Качественное определение в данном методе, так же как и в ТСХ, выполняется или по хроматографическим характеристикам (площади пятна на хроматограмме и интенсивности его окраски), или по методу вымывания. Методами бумажной хроматографии успешно анализируют смеси катионов в неорганическом качественном анализе, смеси аминокислот и других органических кислот, смеси красителей и т.д.
Газовая и жидкостная хроматография. Методами газовой хроматографии анализируют нефтяные и рудные газы, воздух, продукцию основной химии и промышленности органического синтеза, нефть и продукты ее переработки. Методами жидкостной хроматографии определяют состав нефти, керосина, углеводородов, эффективно разделяют транс- и цис-изомеры, алкалоиды и т.д. Методы анализа успешно используются в медицине, биологии, в технологии переработки древесины, в лесохимии и пищевой промышленности, а также в автоматизации производственных процессов.
Количественный хроматографический анализ основан на измерении различных параметров пика, зависящих от концентрации хроматографируемых веществ – высоты, ширины, площади и удерживаемого объема или произведения удерживаемого объема на высоту пика.
В жидкостной адсорбционной хроматографии, как и в газовой, идентификация веществ производится по характеристикам удержания, а количественный анализ основан на измерении высоты или площади хроматографического пика.
Основными в количественной хроматографии являются методы: простой нормировки, нормировки с калибровочными коэффициентами, внутренней стандартизации и абсолютной калибровки. Рассмотрим более подробно метод простой нормировки.
При использовании метода простой нормировки применяют сумму каких-либо параметров пиков, например, сумму высот всех пиков или сумму их площадей за 100%. Тогда отношение высоты отдельного пика к сумме высот или отношение площади одного пика к сумме площадей, умноженное на 100, будет характеризовать массовую долю (%) компонента в смеси. Вполне понятно, что такой метод предполагает существование одинаковой зависимости величины измеряемого параметра от концентрации для всех компонентов смеси.
Пример: Определить массовую долю (%) гексана в смеси гексен-1 и гексан, если их площади хроматографических пиков равны: S1=5 и S2=10 см2, соответственно.
Решение: Сумму их площадей применяем за 100%. Тогда массовая доля (%) гексана в указанной смеси вычисляется по формуле:
 (1)
(1)
где: S1 – площадь хроматографического пика гексена-1;
S2 – площадь хроматографического пика гексана.
Подставляя значение S1 и S2 в уравнение (1):
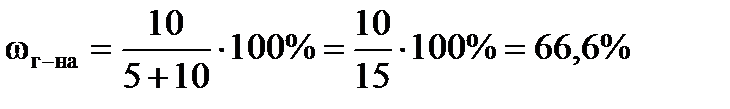

В таблице 20 предложены задания для самостоятельного выполнения.
Таблица 20
Определить массовую долю (%) каждого вещества в указанной смеси, используя приведенные значения площадей хроматографических пиков (S)
| № | Смеси веществ (углеводородов) | Значение площадей хроматографических пиков | ||
| S1 | S2 | S3 | ||
| Пентан – пентен | - | |||
| Пентен – пентин | - | |||
| Пентан – пентин | - | |||
| Пентан – пентен – пентин | ||||
| Гексан – гексен | - | |||
| Гексен – гексин | - | |||
| Гексан – гексин | - | |||
| Гексан – гексен – гексин | ||||
| Гептан – гептен | ||||
| Гептен – гептин | ||||
| Гептан – гептин | ||||
| Гептан – гептен – гептин | ||||
| Октан – октен | ||||
| Октен – октин | ||||
| Октан – октин |
|
из
5.00
|
Обсуждение в статье: Проверка домашнего задания. Обобщение и систематизация полученных знаний |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

