 |
Главная |
Применение экстракционных процессов в технологии урана
|
из
5.00
|
Экстракция неорганических веществ получила распространение сравнительно недавно: использование этого процесса для извлечения и очистки неорганических солей и кислот связано с возникновением и бурным развитием урановой промышленности. В конце 1930 и начале 1940-х для получения урана ядерной чистоты стали использовать извлечение нитрата уранила диэтиловым эфиром. Широкое развитие экстракционной технологии и исследований в области экстракции неорганических веществ относится к началу 50-х годов ХХ века, когда были синтезированы новые экстрагенты, отвечающие требованиям технологии. С тех пор экстракционные процессы завоевали прочное место в технологии урана, при переработке облученного ядерного горючего, в производстве редких металлов.
Экстракционные процессы имеют ряд преимуществ перед осадительными, сорбционными и другими процессами очистки и разделения: они легко автоматизируются, отличаются большой производительностью, открывают возможность создания непрерывных схем. Синтез новых, более дешевых экстрагентов, привел к тому, что в последние годы экстракция начинает занимать ведущее положение в гидрометаллургии цветных и редких металлов. Наличие широкого спектра разнообразных экстрагентов в настоящее время позволяет применять экстракцию для производства и очистки многих неорганических веществ, например, фосфора, фосфорной и других кислот.
Извлечение урана из водной фазы в органическую происходит за счет химического взаимодействия гидратированных ионов урана с экстрагентом с получением новых соединений, растворимых в избытке растворителя или, что чаще, в смеси экстрагента и инертного растворителя.
Обратный процесс – реэкстракция урана в водную фазу также связан с предшествующими химическими процессами разрушения экстрагируемых соединений. Однако механизм экстракции и реэкстракции может быть различным в зависимости от природы экстрагента и условий осуществления самой экстракции.
Механизм экстракции и реэкстракции сложен и до настоящего времени нет единой научной классификации механизмов экстракции.
Рассмотрим экстрагенты и наиболее характерные для них механизмы по классификации, обычно принятой в технологии, подразделяя на три группы.
I-ая группа – Нейтральные экстрагенты
Экстракция сопровождается образованием сольватов (сольватный механизм экстракции). Экстрагенты – кислородсодержащие растворители: спирты, простые и сложные эфиры, альдегиды, кетоны и нейтральные фосфорорганические соединения.
Примеры: Экстракция уранил-нитрата диэтиловым эфиром (ДЭЭ).
 .(1)
.(1)
2. Экстракция уранил-нитрата трибутил фосфатом
 . (2)
. (2)
Реакции комплексообразования с вытеснением воды из внутренней координационной сферы комплекса, которые можно записать следующим образом:
 . (3)
. (3)
Эти экстрагенты экстрагируют преимущественно из азотнокислых растворов в соответствии с приведенными выше реакциями. Для данной группы кислородсодержащих экстрагентов характерна очень высокая степень растворения (емкость) образующихся сольватов в избытке растворителя, достигающая в некоторых случаях растворимости уранил-нитрата в воде (~56 %), поэтому в экстрагент добавляют органические вещества, стабилизирующие фазу экстракта и замедляющие процесс растворения образующихся сольватных комплексов.
II-группа – Органические кислоты, например, ацетилацетон, теноилтрифторацетон, кислые алкифосфаты.
Кислые алкифосфаты, фосфонаты и фосфинаты образуют с уранил-ионом (а также и с U4+) в органической фазе устойчивые комплексные соединения, в состав которых входят катион из водной фазы и анион органической кислоты. При экстракции уранил-иона моноалкифосфатом протекает реакция
 орг+
орг+ 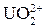 водн
водн 
 орг+ 2H+водн (4)
орг+ 2H+водн (4)
а при экстракции диалкилфосфатом
 орг+
орг+ 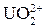 водн
водн 
 орг+ 2H+водн (5)
орг+ 2H+водн (5)
Ионы водорода Н+, освобождающиеся при экстракции, переходят в водную фазу, повышая соответственно ее кислотность. По существу здесь происходит жидкостной катионный обмен, в результате, которого образуются весьма прочные нейтральные комплексные соединения с уранил-ионом в качестве центрального члена и соответствующими органическими лигандами. Эти соединения хорошо растворяются в органической фазе – смеси экстрагента и разбавителя.
Радикалы  и (RО)2РО2 расположены в ряду вытеснительной способности лигандов на первых местах. Они с легкостью вытесняют такие анионы, как Cl-,
и (RО)2РО2 расположены в ряду вытеснительной способности лигандов на первых местах. Они с легкостью вытесняют такие анионы, как Cl-,  ,
,  и др. из внутренней сферы соединений уранила с превращением последних в фосфатные комплексы. В процессе экстракции образуются внутрикомплексные соединения, происходит полимеризация образующихся соединений в органической фазе и процесс осложняется. Поэтому уравнение экстракции уранил-иона ди-2-этилгексилфосфорной кислотой (Д2ЭГФК) можно записать так:
и др. из внутренней сферы соединений уранила с превращением последних в фосфатные комплексы. В процессе экстракции образуются внутрикомплексные соединения, происходит полимеризация образующихся соединений в органической фазе и процесс осложняется. Поэтому уравнение экстракции уранил-иона ди-2-этилгексилфосфорной кислотой (Д2ЭГФК) можно записать так:
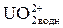 +
+ 

 +
+ 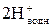 (6)
(6)
С учетом вышесказанного становится ясным, что процесс экстракции кислыми алкилфосфатами идет хорошо из сернокислых, хлоридных, азотнокислых и фосфорнокислых сред, хотя селективность экстрагирования по отношению к урану оставляет желать много лучшего.
III-группа – Органические соединения, для которых растворимость в неполярных растворителях обусловлена образованием солей с органическим катионом.
Поэтому металлы экстрагируются, если они образуют комплексные анионы, к таким экстрагентам относятся, например, органические амины.
Амины – производные аммиака. Первичные  ; вторичные
; вторичные  ; третичные
; третичные  . К аминам относятся также четвертичные аммониевые основания (ЧАО) и их соли:
. К аминам относятся также четвертичные аммониевые основания (ЧАО) и их соли:
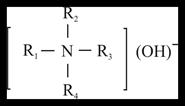
В аминах, как и в аммиаке, азот имеет неподеленную пару электронов, что обуславливает их способность к образованию координационных соединений.
Подобно аммиаку амины реагируют с кислотами, давая соль амина (алкиламмония):
NН3 + НCl → NH4Cl; (7)
R3N + HCl → [R3NHCl]; (8)
2R3N + Н2SO4 → [(R3NН)2SO4]. (9)
Эти соли аминов и служат экстрагентами:
(R3NН)2SO4 + [UO2(SO4)2]2- ↔ [(R3NН)2UO2(SO4)2] +  (10)
(10)
т.е. по существу реализуется анионообменный механизм экстракции, и амины ведут себя подобно анионообменной смоле (только жидкой). В общем случае взаимодействия с амином идет по схеме:
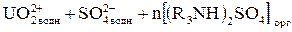 ↔
↔  (11)
(11)
Характерная особенность экстракции аминами – равновесие устанавливается в течение нескольких секунд. Экстракция аминами протекает только в том случае, когда водная фаза содержит ионы водорода в количестве, достаточном для превращения амина в замещенную соль аммония, так как экстрагентами могут быть только соли аминов.
Экстракционная способность аминов увеличивается в ряду:
первичные < вторичные < третичные < четвертичные.
При экстракции урана аминами используют третичные амины (три-Н-октиламин и три-изо-октиламин). Иногда при экстракции урана образуются так называемая третья фаза. Для ее предотвращения надо добавить небольшое количество длинноцепочечного спирта, которое изменяет диэлектрические свойства соли амина.
|
из
5.00
|
Обсуждение в статье: Применение экстракционных процессов в технологии урана |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

