 |
Главная |
Роль адекватной дифференцировки Т-хелперов в обеспечении успешной иммунной защиты (человек)
|
из
5.00
|
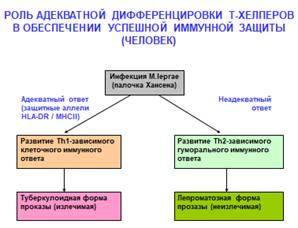
Допустим инфекция палочкой Хансена. Зависит от того, какие конкретно аллели MHC2 присутствуют в организме. Если идет активация Th2-зависимого гуморального ответа, то все плохо, ответ неадекватный (лепроматозная форма проказы). Если активируется Th1-зависимый клеточный иммунный ответ, то развивается туберкулоидная форма проказы (излечимая).
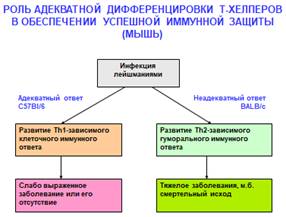
То же есть при лейшманиозах (у мышей).
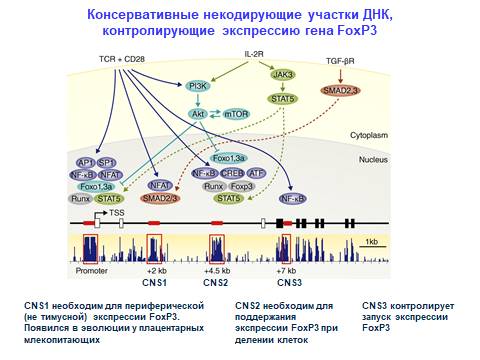
19) Регуляторные Т-хелперы, модульное устройство гена FoxP3.
Регуляторные Т-лимфоциты — центральные регуляторы иммунного ответа. Основная их функция — контролировать силу и продолжительность иммунного ответа через регуляцию функции Т-эффекторных клеток (Т-хелперов и Т-киллеров). У регуляторных Т-клеток CD25 экспрессируется постоянно.
FOXP3 - транскрипционный фактор, необходимый и достаточный для развития регуляторных Т-клеток
Сложно устроенный ген FoxP3 содержит несколько регуляторных участков, интегрирующих сигналы от TCR, рецептора TGFb, и рецептора IL-2.
Ген FoxP3 экспрессируется и в "естествен-ных" (центральных), и в "индуцируемых" (периферических) Treg клетках.
20) Механизмы действия Treg и другие механизмы периферической толерантности.
Механизмы действия Treg:
1. Модификация фенотипа АПК
2. Подавление и уничтожение Т-эффекторов
3. Конкуренция за IL-2.
Механизмы действия регуляторных Т-клеток.
Есть регуляторная Т-клетка, она взаимодействует с АПК, экспрессируя на поверхности CTLA-4 (успешный конкурент СД28), подавляет костимуляцию через B7. Приводит к повышению экспрессии IDO (яркий маркер локальный иммуносупрессии). Приводит к недостатку триптофана, без которого Т-клетки не могут нормально делиться и другой продукт этой реакции - кинуренин, сам по себе обладает иммуносупрессорным действием. Регуляторная клетка может модифицировать фенотип АПК, вызывая подавление экспрессии молекул костимуляции. Может напрямую подавлять и уничтожать эффекторные Т-клетки с помощью цитотоксических механизмов и ТГФ-бета, интерлейкина 10. И еще может конкурировать за ИЛ2. CD25 синтезируется постоянно и хорошо, в отличие от эффекторных.
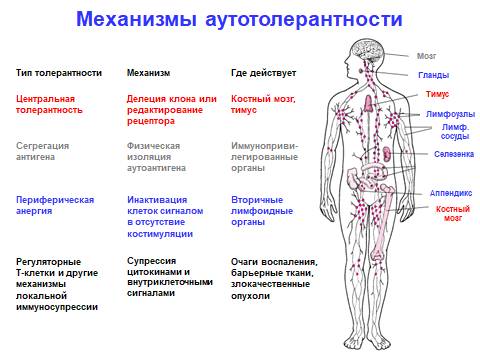

21) Иммунопривилегированные органы. Последствия нарушения целостности гематоэнцефалического барьера.
Иммунопривилегированные органы - появление антигена не приводит к воспалительному иммунному ответу (мозг, глаза, плацента, семенники, щитовидка)
При нарушении целостности ГЭБ - патологические изменения при ишемии головного мозга, проникновение чего угодно в ЦНС.
Система комплемента
1) Особенности С3 как ключевого фактора системы комплемента.
Белок С3 – ключевой фактор системы комплемента.
Его особенность состоит в нестабильности.
Тиоэфирная группа склонна к спонтанному гидролизу
Суть в том, что С3 очень много и у кого-то тиоэфирная связь постоянно спонтанно гидролизуется. Но чтобы реакция распространилась до “взрыва”, необходима реакция тиоэфирной связи с поверхностью частицы. Так реакция стабилизируется. То есть без этого у нас как раз холостая петля.
2) Альтернативный путь активации комплемента.
Центральное звено – «холостая» петля активации C3i>C3b>C3bBb>C3
У белка С3 есть тиоэфирная группа, она может спонтанно гидролизоваться. При этом 2 домена белка С3 (TED и CUB) сильно отодвигаются от остального белка (это теперь С3), освобождая место для посадки фактора В (в присутствии магния). Дальше приходит протеаза D, которая отрезает от фактора В небольшой кусок (Ва), а большая его часть (Bb) остается (в сумме C3iBb). При этом С3 превращается в жидкофазную конвертазу (C3iBb), которая способна гидролизовать другие белки С3 (резать их на С3а - кусок поменьше - и С3b - кусок побольше).
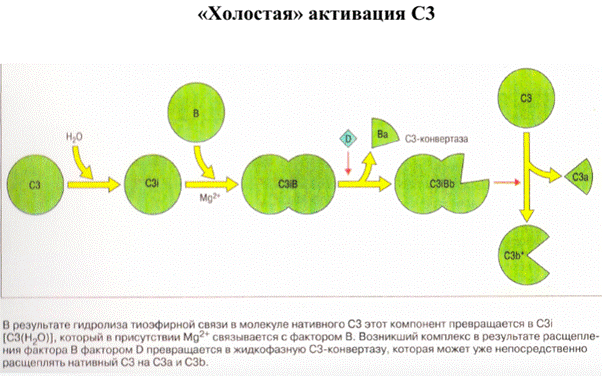
C3iBb отрезает от других С3 домен ANA (он же С3а, так как это маленький кусочек). При этом в С3b происходит похожая конформационная перестройка, как при гидролизе тиоэфирной связи в первом случае. Но здесь эта связь свободна, и она может реагировать с OH- и NH2-группами на поверхности бактерий. На освободившуюся после отщепления С3а площадку опять же садится фактор В, протеаза D отщепляет от него кусок (Ва), в итоге получаем твердофазную конвертазу C3bBb, которая может резать другие С3 на С3а и С3b. Комплекс C3bBb нестабилен, его удерживает пропердин.
Суть в том, что С3 очень много и у кого-то тиоэфирная связь постоянно спонтанно гидролизуется. Но чтобы реакция распространилась до “взрыва”, необходима реакция тиоэфирной связи с поверхностью частицы. Так реакция стабилизируется. То есть без этого у нас как раз холостая петля.
Это альтернативный путь активации комплемента!!!
3) Классический и лектиновый пути активации комплемента.
● Лектиновый путь активации комплемента
В предыдущем пути у нас отрезались маленькие пептиды С3а. Они (и еще С4а и С5а) являются индукторами хемотаксиса и воспаления. Если реакция продолжается, то цитокины из очага воспаления попадают в кровь и в печени вызывают выделение маннан-связывающего лектина (MBL - mannan-binding lectin). Лектин - белок, который связывается с углеводом. MBL состоит из нескольких субъединиц, заканчивающихся головками на ножках (головок всего 4, 5 или 6). Эти головки связывают маннозу на поверхности бактерий (известно, что у человека олигосахариды на поверхности клеток не заканчиваются маннозой, а у бактерий заканчиваются).
Между ножками у MBL две неактивные сериновые протеазы: MASP1 и MASP2 (MASP - mannan-binding protein associated serine protease). Когда головки MBL движутся и связывают остатки маннозы, его ножки разъезжаются, и эти протеазы активируют друг друга. Теперь они могут резать С4 (аналог С3) и С2 (аналог фактора В), в результате чего получается конвертаза С4bС2а, которая может резать С3. Внимание! У С2 перепутаны обозначения букв а и b: у него более большая часть C2а, а маленькая - C2b. У всех остальных наоборот.
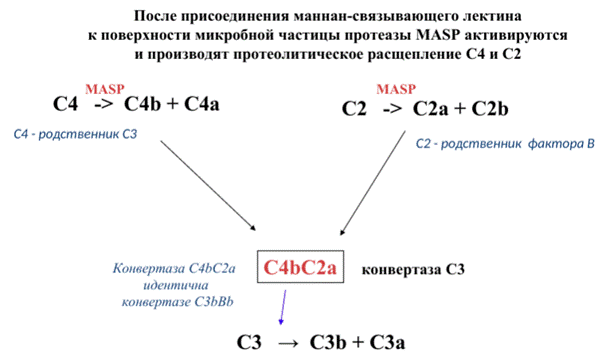
● Классический путь активации комплемента
Очень похож на лектиновый путь. Главный участник - белок C1q - устроен так же, как MBL. Его головки связываются с антителами IgG или IgM, при этом его ножки движутся, что приводит к активации протеаз Clr и Cls - они аналогичны протеазам MASP 1 и 2 и тоже режут С4 и С2.
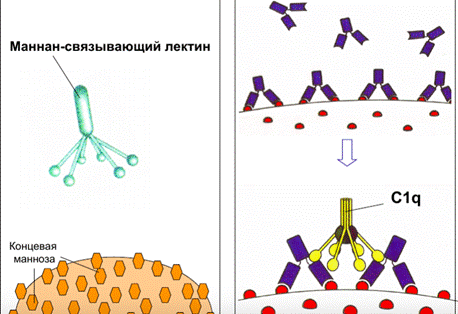
Пусковые факторы (поверхность частицы; микробная поверхность, покрытая множеством остатков маннозы; поверхность, покрытая антителами IgG или IgM)
● Чтобы пошла цепная реакция по альтернативному пути активации комплемента, необходима поверхность частицы с OH- и NH2-группами, чтобы тиоэфирная связь С3b могла связаться с ними. Это стабилизирует конвертазу C3b-Bb, запускается цепная реакция образования новых конвертаз, реакция распространяется по поверхности частицы. Без поверхности возможна только холостая петля активации.
● микробная поверхность, покрытая множеством остатков маннозынеобходима для лектинового пути активации комплемента. При связывании головок маннан-связывающего лектина с маннозой двигаются ножки лектина, что приводит к активации расположенных между ножками сериновых протеаз MASP1 и MASP2, которые начинают резать белки С4 и С2. Получившаяся конвертаза С4bC2a может резать С3, что запускает цепную реакцию.
● поверхность, покрытая антителами IgG или IgM- аналогично предыдущему. Связывание головок белка С1q с антителами активирует протеазы C1r и C1s, расположенные между ножками С1q, что приводит к запуску цепной реакции.
4) Защитные функции комплемента (опсонизация микробных клеток, цитолиз микробных клеток, хемотаксические пептиды С5а, С4а, С3а)
● Опсонизация - облегчение фагоцитоза частицы путем прикрепления к ней некоторых молекул (опсонинов). В случае комплемента происходит опсонизация микробных клеток молекулой С3b. У фагоцитов есть рецептор к С3b, что помогает им зацепить бактерию (“крючок”)
● когда на поверхности бактерии очень много C3b, образуется новая конвертаза C3b-Bb-C3b, она режет белок С5 на С5а (малая часть) и C5b (большая часть). С5b объединяется с белками С6, С7, С8, которые вместе образуют мембрану атакующий комплекс. Этот комплекс инициирует сборку поры из 12-14 молекул белка С9. Таких пор образуется много, клетка продырявливается, в поры затекает вода, и клетку просто разрывает (цитолиз микробных клеток).
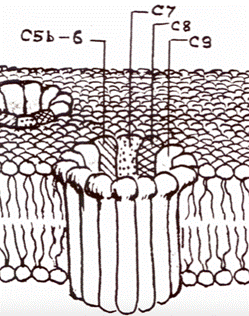
● хемотаксические пептиды С5а, С4а, С3а - малые пептиды, которые отрезаются от соответствующих белков при образовании конвертаз. Так как это разрезание происходит у поверхности, то получается хемотаксический градиент из этих пептидов с максимальной концентрацией у поверхности. У фагоцитов есть рецепторы на эти пептиды (на С3а хемокиновый рецептор - 7 раз пронизывающий мембрану)
5) Факторы, защищающие собственные клетки от системы комплемента.
● фактор I - сериновая протеаза, режет C3b и C4b (этому способствуют Н, MCP, C4BP, CR1)
● фактор Н - связывается с C3b, вытесняя Bb. Способствует разрезанию С3b протеазой I
● CR1 (Complement-receptor 1) и MCP (membrane co-factor protein) - ускоряют разрушение C3b и C4b протеазой I
● C4BP (C4-binding protein) - связывается с C4b, вытесняя C2а. Способствует разрезанию C4b протеазой I
● C1INH (C1 inhibitor) - связывается с активными C1r и C1s, отщепляя их от C1q
● CD59 (протектин) - связываясь с С8 в составе комплекса C5b-C8, не дает связываться белку С9, то есть не дает образовать пору; мембранный белок
● DAF (decay accelerating factor) - заякорен в мембране, ускоряет отсоединение Bb от С3b, C2a от C4b
|
из
5.00
|
Обсуждение в статье: Роль адекватной дифференцировки Т-хелперов в обеспечении успешной иммунной защиты (человек) |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

