 |
Главная |
Ревизионное эндопротезирование тазобедренного сустава и его анестезиологическое обеспечение
|
из
5.00
|
Наряду с ростом абсолютного числа операций тотального эндопротезирования тазобедренного сустава отмечено увеличение доли ревизионного протезирования, что объясняется определенным количеством неудач, как и при любом другом сложном хирургическом вмешательстве (Корнилов Н.В. с соавт., 1995).
К 1995 г сотрудники РосНИИТО им. Р.Р. Вредена располагали наибольшим в стране опытом эндопротезирования тазобедренного сустава. Почти у половины больных (41,24%) был установлен тотальный, разборный, металлокерамический эндопротез тазобедренного сустава разработанный Российским Центром эндопротезирования крупных суставов на базе РНИИТО им. Р.Р. Вредена совместно с фирмой "Феникс". ЭП ТБС Феникс представлял собой единственную отечественную конструкцию, разрешенную Комитетом по новой технике к серийному промышленному выпуску для широкого клинического применения. Именно поэтому анализ осложнений, наблюдавшихся при его использовании, и особенности последовавших ревизионных оперативных вмешательств вызывали наибольший интерес.
На 380 имплантаций эндопротеза ЭП ТБС с 1991 г. по 1995 г. было выявлено 148 различных осложнений, потребовавших хирургической ревизии; при этом 27 больных имели несколько осложнений. Повторяемость части осложнений потребовала внесения конструктивных изменений и замены материалов эндопротеза. Ревизионное эндопротезирование выполнено 121 больному.
В серии наблюдений В.А. Неверова и С.М. Закари (1997) хирургическая ревизия в сроки от 6 месяцев до 12 лет после имплантации эндопротеза потребовалась 52 из 239 больных (21,8%). У 40 из них ревизия проводилась однократно, причем у одного - на обоих суставах, у 11 - дважды и у одного - трижды на одном и том же суставе. Таким образом, в совокупности выполнено 66 ревизий. В 61 наблюдении был имплантирован новый эндопротез, в трех использован ревизионный вкладыш, в одном произведен артродез тазобедренного сустава и в единственном случае глубокого нагноения - резекционная артропластика по Girdlestone, что в дальнейшем не исключало возможности повторного эндопротезирования.
Независимо от причин, послуживших показанием к реэндопротезированию, хирургам приходится сталкиваться с одними и теми же проблемами.
Первой проблемой является подготовка больного к операции и выбор адекватного анестезиологического пособия, принимая во внимание общее состояние, возраст, повторность вмешательства при наличии обширных рубцовых изменений мягких тканей и остеопороза, а нередко и деструкции костной ткани (Корнилов Н.В. и др. 1995).
Вторая особенность ревизионной операции в нередко возникающих сложностях удаления элементов конструкции ЭП, подлежащих замене. Технические трудности могут возникать как при замене одного из компонентов, так и при замене эндопротеза целиком, как при безцементной, так и при цементной его установке. Успех этого этапа операции решают инструменты, специально изготовленные применительно к конструктивным особенностям примененного эндопротеза (Корнилов Н.В., 1995; Неверов В.А., 1997).
Следующей проблемой может стать выбор конструкции и размеров ревизионного эндопротеза, что, в свою очередь, зависит от состояния костного ложа - наличия и величины дефекта костной ткани или ее деструкции, степени остеопороза, наличия перелома бедренной кости, крыши или дна впадины, перелома ножки эндопротеза и кривизны бедренной кости (Корнилов Н.В., 1995).
Как уже было отмечено, ревизионное эндопротезирование характеризуется значительно большей травматичностью, большей продолжительностью хирургического вмешательства и кровопотерей. При его осуществлении резко увеличивается частота как интра -, так и послеоперационных осложнений.
По мнению В.А. Неверова ревизионное эндопротезирование - серьезнейшее оперативное вмешательство, имеющее совершенно особую философию, специфические технологии выполнения операции в условиях дефицита костной ткани, иные конструкции имплантатов и инструментария.
Данное вмешательство требует исключительного внимания ко всем его деталям и тщательного планирования. При всем многообразии неожиданностей, которые встречает хирург во время ревизионного эндопротезирования, следует иметь четкий план оперативного вмешательства, не допускающий методических блуждании, но и не исключающий творческого подхода (Неверов В.А., 1997).
Из-за высокой сложности реэндопротезирования эта операция должна выполняться в специализированных центрах опытными хирургами, знакомыми со всеми последствиями неудавшегося эндопротезирования тазобедренного сустава (Корнилов Н.В., 1997; Неверов В.А., 1997).
Наиболее типичными представляются следующие ситуации (Воронцов С.А. с соавт., 1996).
Одним из наименее сложных вариантов ревизионной операции можно считать замену вкладыша при его разрушении, требующую только обнажения эндопротеза, вывиха его головки и имплантации нового полиэтиленового компонента.
При разрушении вертлужного компонента, отсутствии выраженного остеопороза или патологического остеолиза, достаточной толщине дна и стенок впадины производится замена его на больший типоразмер. При невозможности прочной бесцементной фиксации, устанавливается чашка меньшего размера на цементе.
В случае перелома ножки эндопротеза наибольшую сложность может представлять удаление дистального её отломка. Дистальный фрагмент может быть удален ретроградно с использованием трепанационного отверстия и специального инструмента-толкателя (Корнилов Н.В. с соавт.,1995). При остеопорозе или сопутствующем переломе диафиза во избежание дополнительного ослабления бедренной кости, дистальный фрагмент ножки может быть низведен и удален через коленный сустав, или выбит ретроградно толкателем через межмыщелковую область. При отсутствии зоны резорбции вокруг ножки и предполагаемых трудностях при ее удалении осуществляется трепанация диафиза на протяжении.
Замена эндопротеза целиком производится с цементной или гибридной фиксацией компонентов. Самым травматичными вариантами представляются ревизионные вмешательства при замене конструкции ранее установленной на цемент и/или при наличии широкой зоны деструкции костной ткани вокруг имплантата.
В связи с высокой травматичностью ревизионных операций на тазобедренном суставе адекватность защиты больного от ноцицептивных воздействий, как в ходе вмешательства, так и в после операционном периоде приобретает особое значение.
Наиболее распространенным видом анестезиологического пособия при ревизионных операциях остается многокомпонентный наркоз с искусственной вентиляцией легких газонаркотической смесью и добавлением препаратов нейролептаналгезии, который постепенно вытесняется общей анестезией с преимущественно внутривенным введением препаратов.
В РосНИИТО им. Р.Р. Вредена для обеспечения ревизионных операций на тазобедренном суставе успешно используется метод комбинированной анестезии, включающий различные регионарные блокады и элементы гипноанальгезии субнаркотическими дозами калипсола и препаратов нейролептаналгезии.
Как показал анализ течения операционного периода, комбинированная анестезия обеспечивала полную защиту больного от хирургической агрессии. Гемодинамические показатели отличались стабильностью, что позволяло использовать умеренную гемодилюцию (Ht 32-34%) на фоне медикаментозной гипотонии (клофелин, нитроглицерин).
Реэндопротезирование, в большей мере, чем другие вмешательства на крупных суставах, сопряжено с возможностью значительной кровопотери. При большинстве ревизионных операций показано сочетание предоперационной заготовки аутокрови с интра- и послеоперационным возвратом аутоэритроцитарного концентрата системой Cell Saver.
В рамках настоящего руководства не предполагалось изложения технических деталей и методических особенностей осуществления того или иного вида анестезиологического пособия. При дальнейшем изложении основное внимание обращено на особенности течения данных оперативных вмешательств, наиболее специфической из которых представляется синдром имплантации.
Имплантационный синдром
При эндопротезировании крупных суставов нижних конечностей интравазация жира, содержимого костномозговой полости бедренной или большеберцовой кости, воздуха, а при цементной фиксации компонентов и продуктов неполной полимеризации костного цемента представляет собой непременную составную часть оперативного вмешательства (Корнилов Н.В., 1996).
G. Huemer с соавторами (1995) считают доказанным тот факт, что поступление в кровообращение костного мозга и легочная эмболия встречаются в процессе любой операции замещения тазобедренного или коленного суставов искусственным.
Публикации о жировой и костной эмболии, инфарктах миокарда после тотального эндопротезирования тазобедренного сустава появились с начала семидесятых годов прошлого столетия (Gresham G.A., 1971; Sevitt S., 1972; Herndon J.H., 1974). В 80-90-е годы сообщений о случаях жировой эмболии при эндопротезировании крупных суставов, преимущественно нижних конечностей появлялось все больше (Hagley S.R., 1986; Orsini E.C., 1986; Dorr L.D., 1989; Arroyo J.S., 1994; Byrick R.J., 1994; Johnson M.J., 1996; Richards R.R., 1997).
Дальнейшее накопление знаний позволило поместить жировую эмболию в общую категорию тканевых (паренхиматозных) эмболий. Как постулировал R.Park (1914), паренхиматозная эмболия возможна при фрагментации тканей, наличии доступа в центральную циркуляцию и нарушении гидравлического равновесия, допускающем “интравазацию” тканевых фрагментов.
Тканевую эмболию, приводящую к смерти пациента, может вызывать как первичное, так и ревизионное эндопротезирование.
Патогенез жировой эмболии при эндопротезировании ТБС. Жировая эмболия известна как распространенное осложнение повреждений организма человека различными факторами внешней среды и вследствие заболеваний, обусловленное изменением физико-химических свойств транспортных форм жиров плазмы с последующей эмболизацией сосудов малого и большого кругов кровообращения.
Продолжающаяся дискуссия об источнике эмболического жира касается в основном факторов, нарушающих эмульсионную стабильность жиров плазмы и ведущих к появлению в венозном кровотоке капель, размер которых допускает обтурацию легочных артериол и капилляров, а количество превышает способность легких очищать кровь путем липодиереза (Кустов В.М., 1997).
Эмульсионная стабильность жира плазмы зависит от состояния ее белков (фосфатидов), нарушение обмена которых, изменяя поверхностное натяжение капель жира, приводит к слиянию и укрупнению последних. Отличительным признаком дезэмульгирования является закономерно обнаруживаемая жировая гиперглобулемия - повышенное содержание увеличенных в размерах жировых капель (глобул), что имеет место как при переломах крупных костей, так и при ортопедических вмешательствах на суставах конечностей.
После появления таких глобул в течение более или менее продолжительного времени происходит эмболизация микрососудов бассейна легочной артерии. На начальном этапе она может быть обнаружена только при гистологическом исследовании с использованием специальных способов выявления жира и носит характер патологоанатомического феномена. При продолжающемся поступлении глобул и увеличении количества выключенных из кровообращения сосудов становится возможным с помощью чувствительных методов установить расстройство газообмена и увеличение внутрилегочного шунта без клинической симптоматики, что трактуется как патофизиологический феномен жировой эмболии, отличающийся от патологоанатомического наличием выявляемых изменений гомеостаза.
При субклинических формах жировой эмболии имеются нечеткие симптомы нарушения функционирования сердечно-сосудистой системы и легких, наличие и выраженность которых могут трактоваться и как проявления самого повреждения (заболевания).
Только при выключении из газообмена значительного объема легочной ткани или при повышении сопротивления кровотоку, сказывающемся на нагнетательной функции правого желудочка сердца, появляется клиническая симптоматика.
Иногда клинические проявления наступают сразу вслед за эмболизацией жиром, высвобожденным из мест повреждения жировых депо. Этот компонент образования эмболического жира явно присутствует при абсолютном большинстве механических, барометрических, термических травмирующих воздействий, ведущих к жировой эмболии, а также при заболеваниях, связанных с накоплением жира в клетках отдельных органов или плазме крови.
По всей вероятности, свободный жир, присутствующий в кровотоке в виде капель, лишенных белковой оболочки, вызывает активизацию ферментных систем, что в свою очередь нарушает эмульсионную стабильность транспортных форм жира плазмы и, возможно, наряду с этим усиленный липолиз депонированного жира.
Все перечисленные факторы в совокупности ведут к жировой гиперглобулемии и жировой эмболии сосудов малого и большого кругов кровообращения.
При благоприятном стечении обстоятельств, эффективной профилактике и результативной превентивной терапии происходит разрешение жировой гиперглобулемии путем ферментативного расщепления эмболического жира, восстановления обычного эмульсионного состояния жиров плазмы, откладывания жира в депо, трансформации и выделения. Таким образом завершается большинство субклинических случаев жировой эмболии, в частности при переломах длинных трубчатых костей.
Появление при нарастающей или сохраняющейся гипоксемии со значительным альвеоло-артериальном различием по кислороду явных симптомов жировой эмболии соответствует клиническим её формам.
Необходимо по возможности четко разграничивать симптомы жировой эмболии малого и большого кругов, выделяя те из них, которые характеризуют поражение артериального сосудистого русла. Ограничение представления о клинической жировой эмболии только наблюдениями, при которых имеется типичная петехиальная сыпь или мозговые проявления, вносит определенные искажения в цифры, характеризующие её распространенность, занижая их. С другой стороны, если устойчивую артериальную гипоксемию использовать в качестве единственного или основного признака тканевой (жировой) эмболии, возможна неоправданная гипердиагностика.
Диагноз жировой эмболии предполагается по клиническим признакам, подтверждается лабораторными данными, специальными исследованиями и динамикой процесса, доказывается морфологическими приемами. Развернутый диагноз включает причину развития ЖЭ, преимущественную локализацию поражения, фазу или стадию процесса.
Классификация по этиологическому принципу позволяет из тканевой эмболии вычленить жировую. При явной связи последней с механическими или термическими повреждениями допустимо добавление определения "посттравматическая".
В зависимости от преимущественной локализации жировых эмболов, которая иногда меняется по мере развития осложнения, выделяют легочную или генерализованную формы. Начинаясь с обтурации артериол и капилляров, жировая эмболия проходит механическую фазу, на которой может и завершиться. Однако при ферментативном гидролизе эмболического жира образуются токсичные свободные жирные кислоты, а в процессе разрушения форменных элементов крови и паренхимы высвобождаются биологически активные вещества, что обусловливает развитие химической фазы и возникновение воспалительной реакции.
Практически на любой стадии процесса возможно спонтанное или обусловленное терапией обратное его развитие либо при исчерпании компенсаторных возможностей сердечной или дыхательной систем резкое критическое ухудшение состояния пациента с фатальным исходом.
Ступенчатая (каскадная) теория патогенеза (рис 1), допускающая участие на разных этапах различных патофизиологических механизмов повреждающего воздействия, позволяет использовать в определенный момент при лечении конкретного больного наиболее действенное сочетание терапевтических воздействий, лекарственных средств и препаратов (Кустов В.М., 2002).
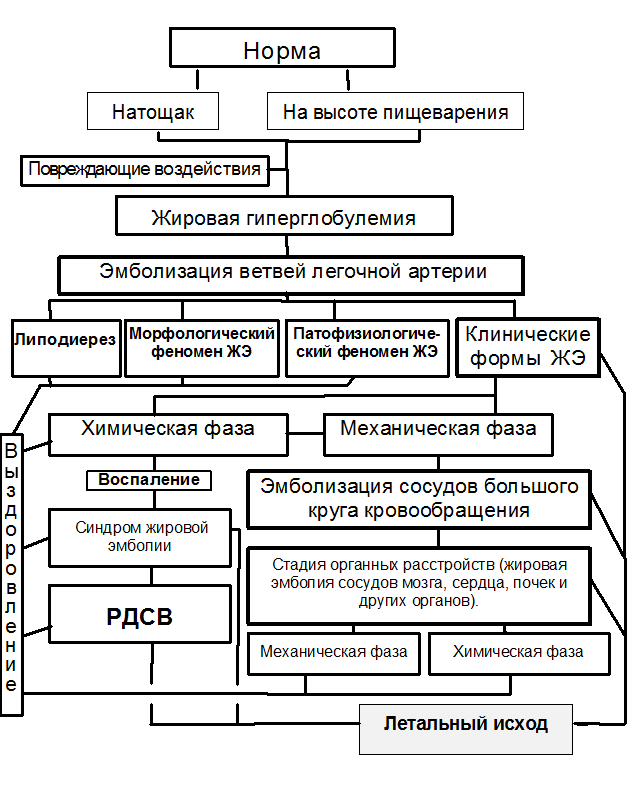
Рис 1. Структурная схема патогенеза ЖЭ
При ортопедических операциях постоянно наличествуют факторы, способствующие проявлению, как патофизиологического феномена, так и клинических проявлений жировой эмболии. К ним следует отнести:
* нарушение целости кости и разрушение на большом протяжении содержимого костномозгового канала;
* отсутствие способности к спадению и зияние сосудов кости, широкий просвет её вен;
* жировое перерождение костного мозга с возрастом и изменение консистенции внутрикостного жира;
* нежность жировых клеток костного мозга.
Сразу же после разреза подкожной жировой клетчатки хорошо видимые капли жира появляются в ране. После рассечения кости значительно большее количество крупных жировых капель стекает в рану, и показывается тающий при прикосновении к нему жировой костный мозг (Peltier L.F., 1984).
Во время обработки костномозговой полости резкое повышение костномозгового давления в ходе рассверливания сопровождается интравазацией поврежденной ткани костного мозга. Повышение внутрикостного давления при имплантации бедренного компонента эндопротеза на цементе доказано экспериментальными и клиническими исследованиями (Rinecker H., 1980; Marshall P.D.., 1991; Kolettis G.T., 1994; Martin R., 1996; Richards R.R., 1997).
Биологически это давление уравнивается посредством венозной дренажной системы, расположенной в linea aspera и дистальном метафизе. Интравазация костного мозга, жира и “дебриса” ведет к характерным клиническим признакам более или менее заметной эмболии легкого, которая проявляется интраоперационно падением кровяного давления и pCO2 конца выдоха. Чтобы избежать биологического самодренажа, логично обеспечить достаточное дополнительное дренирование костномозговой полости бедренной кости через транскортикальное вентильное отверстие дистальнее предполагаемого нахождения кончика ножки протеза, наряду с помещением в канал костной пробки, в тех случаях, когда цемент подается под высоким давлением. Если создать вакуум в костномозговой полости, чтобы цемент втягивался в губчатую кость, можно ожидать оптимального результата цементирования в сочетании с минимальным риском для пациента (Ulrich С., 1995).
В эксперименте установлено, что основная часть жировых эмболов формировалась именно при работе сверлом-разверткой, а не вследствие повышения интрамедуллярного давления, роль которого второстепенна (Wozasek G.E., 1994).
При эндопротезировании тазобедренного или коленного суставов увеличение внутрикостного давления стимулирует выход костного мозга в кровяное русло более чем у 90% пациентов. При этом 3-4% из них демонстрируют синдром жировой эмболии с вовлечением легких, мозга и петехиальными высыпаниями; приблизительно у каждого пятого возможно его молниеносное и фатальное течение (Kratochwill C., 1995). Жировые капли из места операции достигают правого предсердия в течение тотального эндопротезирования тазобедренного сустава (Jones R.H., 1975).
Ультразвуковой инструмент, применяемый при ревизионных вмешательствах, отличается повышенной способностью образовывать большие потоки эмболов, особенно во время извлечения дистальной порции цемента. При достаточных компенсаторных возможностях сердечно-легочной системы больного изменения гемодинамики могут быть минимальными и оставаться на субклиническом уровне, но, если пациент ослаблен, ситуация может стать угрожающей для его жизни. Учитывая подобный механизм усугубления эмболизации при реэндопротезировании тазобедренного сустава, можно уменьшить вероятность жировой эмболии (Woo R., 1995).
A.W. Elmaraghy с соавторами (1998) установили, что присутствие мономера метилметакрилата не оказывало никакого влияния на распространенность или гемодинамические проявления легочной жировой эмболии, обусловленной рассверливанием и обработкой костномозгового канала бедренной кости. Результаты их направленного исследования не подтвердили гипотезу, согласно которой костный цемент на основе MMA вызывает агглютинацию хиломикронов плазмы, способствующую легочной жировой эмболии.
Для повышения качества цементной мантии костный цемент подают под высоким давлением с использованием цементного пистолета и обтуратора, помещенного в верхний отдел костномозговой полости бедренной кости. Однако, как показал приведенный P.D. Marshall с соавторами (1991) случай фатальной жировой эмболии, такие приемы не свободны от осложнений.
В статье P.W. Pinto (1993) проанализированы некоторые вероятные причины побочных эффектов костного цемента при ортопедических операциях. Они включают эмболию жиром, воздухом, тканью костного мозга, периферическую вазодилятацию, активацию каскада свертывания в пределах легких, прямое сердечно-сосудистое депрессивное влияние костного цемента или мономера метилметакрилата.
J.S. Arroyo с соавторами (1994) сообщили о случае жировой эмболии при бесцементной имплантации биполярного эндопротеза, закончившейся смертью больного.
D. Galdermans с соавторами (1989) представили пациентку с прогрессивной дыхательной недостаточностью, вызванной легочной жировой эмболией, что было засвидетельствовано открытой биопсией легкого. За четыре с половиной года до этого ей было выполнено внутрисуставное эндопротезирование тазобедренного сустава на костном цементе. Авторы предположили, что эмболизация костным мозгом была обусловлена асептическим рассшатыванием имплантата.
Риск жировой эмболии возрастал при использовании внутрикостной фиксации компонентов тотального эндопротеза. Для его снижения должны использоваться рифленые ножки и вентильные отверстия (Dorr L.D., 1989).
В начальном периоде освоения эндопротезирования ТБС была выявлена следующая закономерность. При нарушении целостности кости (и мягких тканей) в ходе оперативного вмешательства и особенно при введении в костномозговой канал бедренного компонента эндопротеза и цемента под давлением отмечено развитие “синдрома имплантации. Косвенными признаками этого служили изменения гемодинамики и газообмена, выявленные при интраоперационном мониторном наблюдении. Иногда гипотония после рассверливания костномозгового канала бедренной кости возникала и без последующего внедрения цемента. При этом не было отмечено нарушений ритма сердечных сокращений и признаков гипоксии миокарда. Это побудило исследовать причины гемодинамической нестабильности.
Анализ результатов наблюдений показал, что продуктам неполной полимеризации костного цемента не принадлежит основная роль в возникновении описанных проявлений. Вероятной их причиной послужила микроэмболия ветвей легочной артерии. Попадание в кровоток жира костного мозга с последующим слиянием мельчайших капель жира, присутствующих в плазме в виде эмульсии, совместно вызывало появление крупных капель, способных закупорить сосуды.
Частота клинически выраженной жировой эмболии составила, по нашим данным 17 случаев на 339 операций экстренного однополюсного эндопротезирования, 2 случая на 412 операций тотального эндопротезирования ТБС в плановом порядке и 3 на на 110 ревизий ранее установленного эндопротеза.
На 977 операций эндопротезирования тазобедренного и коленного суставов пришлось 12 смертельных исходов, связанных с жировой гиперглобулемией и эмболией, что свидетельствует о реальной опасности развития тяжелых, иногда жизнеопасных осложнений, обусловленных нарушениями жирового обмена и эмульсионной способности жиров плазмы при этих вмешательствах.
В трех случаях этого осложнения, приведшего к смерти в первые 30 часов после тотального и однополюсного эндопротезирования тазобедренного сустава, обнаружены выраженная гипоксемия, гиперкапния, элементы массивной жировой эмболии (секционный материал[1]) сосудов легких, почек и миокарда (рис 2, 3, 4).
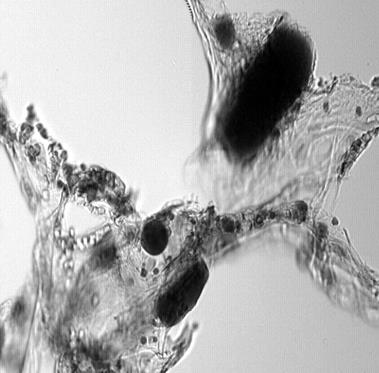
Рис 2. Жировая эмболия сосудов легких
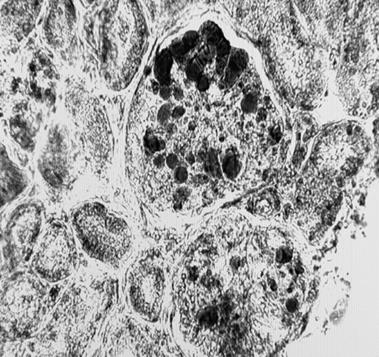
Рис 3. Жировая эмболия сосудов клубочка почек
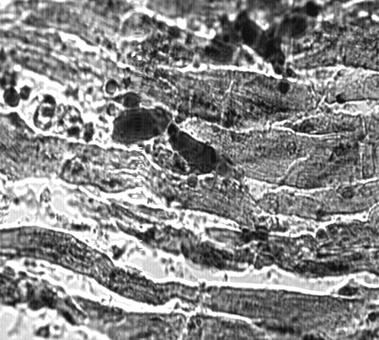
Рис 4. Жировая эмболия сосудов миокарда
Эффективным способом обнаружения феномена гиперглобулемии служат методики, основанные на определении размеров и числа жировых глобул в сыворотке и плазме крови путем микроскопирования после предварительной их окраски (Лиепа М. Э., 1967, 1973; Апанасенко Б. Г., 1976; Bschoor F., 1963).
Для выявления жира исследовали цитратную плазму крови на различных этапах эндопротезирования используя краситель судан - III и микроскопию в проходящем свете. Количество жировых капель диаметром более 8 микрон подсчитывали при увеличении в 280 раз (Кустов В. М., Перфилетова П. Е., 1998). Через три минуты после внедрения бедренного компонента эндопротеза тазобедренного сустава в 12 из 16 случаев выявлена выраженная жировая гиперглобулемия, интенсивность которой в 2 - 3 раза превышала результаты определения жировых глобул в плазме тех же пациентов, взятой до операции.
Анализ полученных данных позволил установить следующее:
у абсолютного большинства больных после обработки костномозговой полости в крови обнаруживается значительное количество жировых капель;
после внедрения бедренного компонента эндопротеза число их возрастает;
после установки обоих компонентов увеличивается количество жировых капель с повышенной адгезией к стеклу;
в отдельных случаях существенная жировая гиперглобулемия имеется при отсутствии клинических проявлений ЖЭ;
удается выявить в плазме крови суданофильные включения плотной консистенции, на поверхности которых имеются мелкие капли жира.
Профилактика жировой эмболии. На стадии предшествующих жировой эмболии патологических изменений профилактические меры должны быть направлены на устранение факторов, способствующих проникновению жира в кровоток, укрупнению жировых капель, и на снижение рефлекторного ответа на начинающуюся эмболизацию микрососудистого русла малого круга кровообращения.
К хирургическим мерам профилактики жировой эмболии при эндопротезировании крупных суставов конечностей относится применение современных технологий установки имплантатов и конструкций, требующих минимального нарушения целостности содержимого костномозговой полости.
В случаях эндопротезирования тазобедренного сустава в порядке экстренной помощи при переломах проксимального отдела бедренной кости лицам преклонного возраста в связи с выраженным остеопорозом и изменением консистенции жира костного мозга опасность его интравазации особенно велика, что требует использования всех возможных приемов предотвращения избыточного давления в костномозговой полости.
Как при тотальном, так и при однополюсном замещении тазобедренного сустава наибольшую опасность в отношении интравазации жира представляют этапы обработки костномозгового канала бедренной кости, внедрения бедренного компонента эндопротеза, особенно при цементной его фиксации. В последнем варианте обязательно выполнение приемов, препятствующих резкому повышению давления в обработанной полости. Простейшими из них являются: помещение пробки из губчатого вещества удаленной головки бедренной кости ниже кончика внедряемой ножки эндопротеза; введение дренажной трубки до дистальных отделов полости на время подачи цемента.
Особо опасным с точки зрения массивной интравазации жировых капель является промежуток времени от остеотомии до завершения имплантации компонентов эндопротеза. Сильные удары по остеотому при ненарушенной целостности кости могут вызвать поступление жира в вены костного мозга. Вскрытие костномозговой полости бедренной или большеберцовой кости вызывает истечение его наружу, а последующее рассверливание обнажает просветы сосудов как кости, так и костного мозга, открывая доступ в них жидкого жира. Каждое внедрение рашпиля, тест-протеза, костного цемента (особенно шприцем или цементным пистолетом) обусловливает поступление жира, тканевого детрита, воздуха в кровоток.
К хирургическим мерам профилактики жировой эмболии относятся техника оперирования без сильных ударов по неповрежденной бедренной кости, включающая постепенное вскрытие костномозговой полости, удаление жировоперерожденного костного мозга, дренирование её дистальных отделов перед введением костного цемента, а также исключение грубых повторных внедрений сверла, бедренного компонента эндопротеза, особенно при цементном его креплении.
При обработке костномозговой полости и внедрении инструментов (сверла, развертки, рашпили), тест-протезов и компонентов искусственного сустава необходимо избирать щадящие приемы. Перед внедрением цемента необходимо дренированием дистального отдела костномозговой полости предотвратить пиковое повышение внутрикостного давления. Все погружные конструкции следует вводить медленно.
При ревизионном эндопротезировании, насколько можно судить по данным литературы, опасность эмболизации жиром меньше в связи с облитерацией сосудов костномозговой полости. Однако наш опыт свидетельствует о высокой вероятности развития тяжелой интраоперационной жировой эмболии при замене нестабильного эндопротеза как тазобедренного, так и коленного сустава.
Для профилактики интравазации костных, костномозговых фрагментов и жира большое значение имеет исключение гемодинамической нестабильности и резкого снижения центрального и местного венозного давления особенно в момент внедрения компонентов эндопротеза, что часто совпадает с пиком интраоперационной кровопотери, гиповолемии, сокращением венозного притока со снижением уровня центрального венозного давления или без этого. Все перечисленные изменения гемодинамики могут способствовать попаданию в кровоток тканевых фрагментов и жира.
Поддержание достаточного уровня волемии, обеспечение стабильности гемодинамических показателей и адекватное обезболивание являются важными факторами профилактики жировой эмболизации. Свойства инфузионных сред, применяемых для борьбы с гиповолемией, в известной мере определяют эффективность превентивной терапии. Гипертонические растворы глюкозы, особенно в смеси с раствором новокаина, препараты белка (альбумин), в определенной степени декстраны оказывают разнонаправленное защитное действие, снижая выраженность липолиза, препятствуя проявлению токсического влияния свободных жирных кислот и улучшая условия центрального и периферического кровотока.
Непосредственно перед подачей костного цемента стремятся максимально адекватно восполнить кровопотерю кровезаменителями, внутривенно вводят 30 - 90 мг преднизолона; на момент внедрения цемента и бедренного компонента рекомендуется исключить из газонаркотической смеси закись азота.
При признаках массивного поступления микроэмболов в систему легочной артерии стабилизацию артериального давления в отдельных случаях обеспечивает медленная инфузия 120-240 мг эуфиллина.
Поскольку очевидно, что при жировой эмболии первичное поражение сосудов легких является основным фактором патологии, а гипоксемия - прямым следствием обтурации значительной части капилляров и внутрилегочного шунтирования, дополнительная оксигенация выступает в качестве первоочередной симптоматической и заместительной терапии. Особенное внимание в плане поддержания дыхательной функции легких должно быть обращено на пациентов, у которых выявлено значительное снижение парциального давления кислорода в артериальной крови (pO2 a ниже 65 мм рт ст.) или установлена явная гиперглобулемия прямым определением количества и характеристик жировых капель цитратной плазмы венозной крови (6, 8). О высокой выраженности гиперглобулемии при восполненной кровопотере можно судить по значительной тахикардии.
В диагностическом отношении выраженная тахикардия при эндопротезировании крупных суставов не является постоянным симптомом эмболизации мелких ветвей легочной артерии, особенно у больных пожилого и преклонного возраста. Чаще наблюдаются преходящая артериальная гипотония, нарастающая гипоксемия без явной гиперкапнии.
При отсутствии гиперкапнии возможно увеличение содержания кислорода во вдыхаемой смеси до 70 - 80%, однако предпочтительнее использовать концентрацию О2 до 40%, сочетая её при невозможности обеспечить достаточный уровень оксемии с дыханием в режиме положительного давления в конце выдоха.
Из лекарственных средств специфической профилактики на стадии предшествующих патологических изменений и в механической фазе жировой эмболии назначают эмульгаторы - липостабил, эссенциале в профилактических дозах (первоначальная доза 40 мл, поддерживающая - 20 мл 4 раза в сутки).
Большинство исследователей подтвердили высокую профилактическую эффективность стероидных гормонов и их фармакологических аналогов - гидрокортизона, преднизолона, метилпреднизолона, триамцинолона. Для преднизолона рекомендуется начальная доза 60 - 90 мг, метилпреднизолона - до 40 мг и повторное введение их в течение первых трех суток.
Для снятия рефлекторного спазма артериол в бассейне легочных артерий возможно введение ганглиолитиков (пентамин 50 мг) внутривенно капельно или фракционно методом тахифилаксии.
Сердечные гликозиды в обычных терапевтических дозах обеспечивают инотропный эффект без увеличения потребности миокарда в кислороде и в механической фазе преимущественно легочной формы жировой эмболии способны предупредить развитие сердечной недостаточности и способствовать переживанию больным критического периода.
При лечении начальных признаков острой сердечной недостаточности прибегают к допамину и добутрексу в дозе от 3 до 15 мкг/кг/мин.
С профилактической целью и в составе превентивной терапии рекомендованы ингибиторы протеолитических ферментов - контрикал или трасилол по 1 - 2 млн ед/сут; гордокс по 10 - 20 тысяч ед/сут.
Использование этилового спирта и гепарина в раннем периоде после травмы для профилактики жировой эмболии нецелесообразно (Peltier L.F., 1988; Levy D., 1990).
В результате улучшения анестезиологического обеспечения клинические проявления
|
из
5.00
|
Обсуждение в статье: Ревизионное эндопротезирование тазобедренного сустава и его анестезиологическое обеспечение |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

