 |
Главная |
Арилимино-4-хлор-5Н-1,2,3-дитиазолы
|
из
5.00
|
Известно, что соль Аппеля 1а довольно чувствительна к атаке нуклеофилов по атому углерода С(5) гетероцикла. Так, ариламины дают в реакции с 1а 5-арилимино-4-хлор-5Н-1,2,3-дитиазолы 19.[1] Образующийся хлористый водород может быть связан избытком ароматического амина или пиридином. В реакцию вступают практически все известные ароматические и первичные гетероароматические амины, выходы арилиминов, как правило, высокие. Хотя алифатические амины также бурно реагируют с солью 1а, продукты реакции выделены не были. Алкилимины 20 были получены при использовании менее основных бис(триметилсилил)аминов, однако выходы целевых продуктов в этом случае невелики 30-48% (Схема 11).[1, 21]
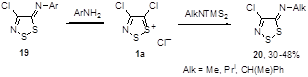
Схема 11
Замещенные в положении 5 тетразолы реагируют с солью Аппеля 1а при комнатной температуре, образуя гидразоноил хлориды 21 с высокими выходами.[22] 5-Аминотетразол взаимодействует более глубоко – с двумя молекулами 1а, давая бис(имино)дитиазол 22. Предполагается, что за атакой атома азота тетразольного цикла на атом углерода соли Аппеля следует раскрытие тетразольного кольца. Если положение N-1 тетразольного цикла заблокировано, то 5-амино-2-алкилтетразолы реагируют с 1а, как и другие ароматические и гетероароматические первичные амины, образуя иминоаддукты 23 с высоким выходом (Схема 12).

Схема 12
Необычный синтез N-винил-1,2,3-дитиазолиламинов из соли Аппеля и азиридинов был недавно предложен Краюшкиным и соавторами.[23] Процесс, очевидно, включает в себя отрыв атомов водорода от атомов азота и углерода. Показано, что реакция этилового эфира или амида азиридинкарбоновой кислоты 24, которые находятся в транс-конфигурации, с солью Аппеля приводит к образованию только одного из возможных изомеров 25 (Схема 13). Очевидно, раскрытие азиридинового кольца происходит практически одновременно с образованием двойной связи.

Схема 13
С целью определения степени взаимодействия двух дитиазольных колец в зависимости от электронных и стерических характеристик связующего мостика из соли Аппеля и гидразина был получен бифункциональный 1,2,3-дитиазол 26 (Схема 14).[24]

Схема 14
Аналоги соли Аппеля 7, полученные из оксима ацетофенона и его 4-нитропроизводного, не выделялись, а переводились в 5-арилимино производные 27 реакцией с ароматическими аминами (Схема 15). [11]

Схема 15
Арилимины могут быть получены и не из соли Аппеля или ее аналогов, а неожиданной реакцией 3,5-дициано-1,2,4-тиадиазола 28 с хлоридами серы (SCl2 и S2Cl2) в присутствии каталитических количеств четвертичной соли Adogen 464, однако выход иминопроизводного 29 невысок (34%) (Схема 16).[25]
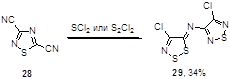
Схема 16
Дитиазол-3-оны
Соль Аппеля 1а быстро разлагается во влажных условиях с выделением хлористого водорода, образуя коричневую массу, из которой дитиазолон 30 может быть выделен сублимацией.[1] Но еще лучше соединение 30 получается реакцией с нитратом натрия в хлористом метилене (выход 72%). Механизм этого интересного превращения предполагает нуклеофильную атаку нитрат аниона по атому углерода С(5) с последующим отщеплением нитроил хлорида (NO2Cl) от промежуточного соединения 31 (Схема 17).[1]

Схема 17
Взаимодействие 1а с карбоновыми кислотами в присутствии 2,6-лутидина при – 78 °С с последующей обработкой спиртом приводит к дитиазолон 30 и эфиру этой карбоновой кислоты.[26] Авторы предполагают промежуточное образование соединения 32, аналогичного интермедиату 31. Было найдено, что первичные спирты дают наиболее высокие выходы эфиров (65-84%), в отличие от вторичных и третичных (39-59%), возможно благодаря стерическим препятствиям при атаке спирта на соединение 32. Эта реакция предлагается как мягкий метод этерификации карбоновых кислот (Схема 18).

Схема 18
4-Фенил-1,2,3-дитиазол-5-он 33 был получен при фотоизомеризации 5-фенил-1,3,2-дитиазол-4-она 34 в различных хлорированных растворителях (CH2Cl2, CCl4).[27, 28] Выходы в этой реакции средние – 40-43%. Предполагается, что образование кетона 33 происходит через бициклический интермедиат 35 (Схема 19).
 Схема 19
Схема 19
Другой метод синтеза кетона 33 включает реакцию промежуточно образующейся из оксима ацетофенона и монохлорида серы соли 1,2,3-дитиазолия 7 c водой, однако выход в этом случае не превышает 33% (Схема 20).[10]
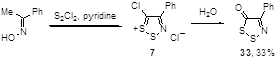
Схема 20
Дитиазол-3-тионы
Обработка соли Аппеля 1а сероводородом в ацетонитриле при комнатной температуре приводит к тиону 36 с 69%-ным выходом.[1] Это же вещество может быть получено при использовании 2-цианотиоацетамида вместо сероводорода в хлористом метилене с 89%-ным выходом (Схема 21).[2]

Схема 21
4-(трет-Бутил)-1,2,3-дитиазол-5-тион 37 был выделен с 2%-ным выходом из реакции трет-бутилацетилида лития и хлорида тетратиатриазепиния 38 (Схема 22).[27]
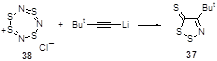
Схема 22
|
из
5.00
|
Обсуждение в статье: Арилимино-4-хлор-5Н-1,2,3-дитиазолы |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

