 |
Главная |
Из оксимов циклических кетонов
|
из
5.00
|
Механизм превращения оксимов циклических кетонов в конденсированные 1,2,3-дитиазолы – реакции, интенсивно исследуемой в последние годы, предполагает образование N-оксида дитиазола. Однако, единственный известный до настоящего времени N-оксид 63 был выделен из реакции стабилизированного двумя трет-бутильными группами оксима циклопентадиенона 64, с монохлоридом серы в тетрагидрофуране при комнатной температуре с 58%-ным выходом (Схема 38).[44]

Схема 38
Во всех других превращениях оксимов циклических кетонов выделяются 1,2,3-дитиазолы, которые, по-видимому, получаются путем деоксигенизации промежуточных N-оксидов под действием S2Cl2. Так, 1-оксимино-3-фенилинден 65 образует дитиазол 66 (Схема 39).[35, 45]

Схема 39
Эта реакция была распространена на оксимы циклопентенона и циклопентанона. Наиболее важным достижением стало применение в этом превращении N-этилдиизопропиламина (так называемого основания Хюнига), которое позволило достичь наиболее высоких выходов дитиазолов 66 (90%) и 67 (25%). Многочисленные реакции хлорирования, дегидрохлорирования и окисления, которые предполагаются авторами в сложном многоступенчатом механизме образования дитиазола 67, делают реакцию чувствительной к малейшим изменениям условий реакции и являются ответственными за невысокий выход конечного продукта. В случае, если карбоциклическое кольцо защищено заместителем (см. образование соединений 63 и 66), хлорирования этого кольца не происходит (Схема 40).[35]

Схема 40
Аналогично протекает реакция и для оксима семичленного циклического кетона, давая смеси хлорированных циклогепта-1,2,3-дитиазолов 68 и 69.[35] Для хлорирования используется 15-ти кратный избыток монохлорида серы и полихлорирование происходит с большим выходом в присутствии N-хлорсукцинимида (NCS) (Схема 41).
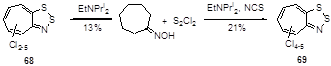
Схема 41
Циклопента-1,2,3-дитиазолиевая система 70 образуется в реакции 2-замещенных оксимов циклопентанона и монохлорида серы.[46, 47] Исчерпывающее хлорирование сопровождает эту реакцию, как и в случае других циклопентадитиазолов (см. выше) (Схема 42).
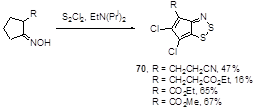
Схема 42
Несколько оксимов циклопентанона, конденсированных с тиофеновым кольцом, были введены во взаимодействие с монохлоридом серы и триизобутиламином в тетрагидрофуране.[47] После 3 дневной выдержки при 4 °С был получен ряд соответствующих тиеноциклопентадитиазолов 71-73 с выходами от средних до высоких (Схема 43).

Схема 43
Этот же подход был применен и для получения пентациклических бис[1,2,3]дитиазоло-s-индаценов 74 и 75 с выходами 46 и 75%, соответственно, из диоксимов 1,5- и 1,7-гидринацендионов 76 и 77.[47] В первом случае реакция осложняется гидролизом одной из оксимных групп, что приводит к получению монодитиазола 78 (Схема 44).
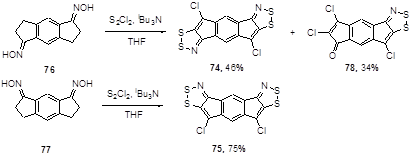
Схема 44
6H-1,2,3-Бензодитиазол-6-оны 79 могут быть получены из бензохинон-4-оксимов, S2Cl2, N-этилдиизопропиламина и NCS.[48] Хлорирование, как обычно, сопровождает образование дитиазольного цикла из оксима; заместители в положениях 2 и 6 бензохинонового цикла остаются неизмененными в продуктах реакции, за исключением трет-бутильной группы, которая замещается атомом хлора. 1,4-Нафтохинон-4-оксим и 1,2-нафтохинон-2-оксим образуют аналогичным образом дитиазолы 80 и 81 (Схема 45).[48]

Схема 45
|
из
5.00
|
Обсуждение в статье: Из оксимов циклических кетонов |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

