 |
Главная |
Гидролиз – реакция взаимодействия соли с водой, приводящая к образованию слабого электролита с изменением характера среды.
|
из
5.00
|
Гидролизу подвергаются соли, образованные слабым основанием и сильной кислотой и наоборот. Соли, образованные сильным основанием и сильной кислотой гидролизу не подвергаются.
Пример:
1. Взаимодействие соли, образованной слабой кислотой и сильным основанием.

 СН3СООNa+ HOH СН3СООH+NaOH
СН3СООNa+ HOH СН3СООH+NaOH
 СН3СОО-+ HOH СН3СООH+OH- , рН > 7, среда щелочная.
СН3СОО-+ HOH СН3СООH+OH- , рН > 7, среда щелочная.
2. Взаимодействие соли, образованной сильной кислотой и слабым основанием.
 NH4Cl+HOH NH4OH+HCl
NH4Cl+HOH NH4OH+HCl
 NH4++ HOH NH4OH+H+, рН<7, среда кислая.
NH4++ HOH NH4OH+H+, рН<7, среда кислая.
3. Взаимодействие соли, образованной слабой кислотой и слабым основанием.


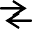 СН3СООNH4 СН3СОО-+ NH4+ СН3СОО-+HOH СН3СООH+OH- NH4++ HOH NH4OH+H+.
СН3СООNH4 СН3СОО-+ NH4+ СН3СОО-+HOH СН3СООH+OH- NH4++ HOH NH4OH+H+.
 СН3СОО NH4+HOH NH4OH+ СН3СООH, рН~7, среда нейтральная. Механизм гидролиза солей заключается в поляризационном взаимодействии ионов соли с их гидратной оболочкой. Чем сильнее это
СН3СОО NH4+HOH NH4OH+ СН3СООH, рН~7, среда нейтральная. Механизм гидролиза солей заключается в поляризационном взаимодействии ионов соли с их гидратной оболочкой. Чем сильнее это
взаимодействие, тем интенсивнее протекает гидролиз.
Все рассмотренные случаи гидролиза касались солей, образованных однокислотными основаниями и одноосновными кислотами. Соли
многоосновных кислот и многокислотных оснований гидролизуются ступенчато, образуя при этом кислые и основные соли.
Например, соли Na2CO3, К3РО4 гидролзуются ступенчато, образуя кислые соли.
Соли AlCl3, Cu(NO3)3, CrCl3 гидролизуются ступенчато с образованием на промежуточных стадиях основных солей.
Процесс гидролиза характеризуется константой гидролиза (Кгидр) и степенью гидролиза (α). Константа гидролиза отвечает за глубину протекания процесса.
Рассмотрим взаимодействие хлорида аммония с водой:
 NH4Cl+H2O NH4OH+HCl
NH4Cl+H2O NH4OH+HCl
 NH4++ H2O NH4OH+H+, рН<7, среда кислая
NH4++ H2O NH4OH+H+, рН<7, среда кислая
Запишем константу равновесия, характеризующую процесс взаимодействия хлорида аммония с водой:
Kравн =
[NH
[
OH][H+ ]
| NH4 |
| H2O |
= Kгидр .
Степень гидролиза представляет собой отношение концентраций гидролизуемой соли к общей концентрации соли и выражают в долях единицы или в процентах:
α =  .
.
Степень гидролиза зависит от природы соли, ее концентрации и температуры.
Согласно закону действующих масс, степень гидролиза возрастает с разбавлением раствора. Качественно влияние температуры на степень гидролиза можно прогнозировать на основе принципа Ле Шателье. Так, реакция экзотермична (∆Н0 = – 56,5 кДж /моль), то противоположный ей процесс гидролиза является эндотермическим.
Поэтому в соответствии с принципом Ле Шателье с повышением температуры степень гидролиза растет.
Гидролиз характерен для многих классов неорганических и органических соединений. Гидролиз неорганических соединений важен для оценки их токсичности, а гидролиз органических соединений применяют для получения ценных продуктов из древесины, жиров, эфиров и т.п., но особенно важную роль гидролиз играет в жизнедеятельности живых организмов.
Роль гидролиза в биохимических процессах трудно переоценить. Прежде всего, необходимо отметить ферментативный гидролиз, благодаря которому три основных компонента пищи - жиры, белки, углеводы - в желудочно- кишечном тракте расщепляются водой на более мелкие фрагменты. В общем виде гидролиз пищевых компонентов описывается
R1 – O – R2 + H2O→ R1 – OH + R2 – OH,
где R1, R2 – фрагменты биоорганической молекулы, связанные через кислород. Без этого процесса не было бы возможно усвоение пищевых продуктов,
так как всасываться в кишечнике способны только относительно небольшие молекулы.
Так, усвоение полисахаридов и дисахаридов становится возможным послетолько полного их гидролиза ферментами до моносахаридов.
Точно так же белки и липиды гидролизуются до веществ, которые лишь потом могут усваиваться.
|
из
5.00
|
Обсуждение в статье: Гидролиз – реакция взаимодействия соли с водой, приводящая к образованию слабого электролита с изменением характера среды. |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

