 |
Главная |
ЗАДАНИЯ ДЛЯ УЧАЩИХСЯ 10 КЛАССА
|
из
5.00
|
ЗАДАНИЕ 1
Задание включает материал по химии углеводородов предельного и непредельного рядов: строение, изомерия и номенклатура, свойства, получение. Решение расчетных задач предполагает использование основных понятий химии: относительная атомная и молекулярная масса, моль, молярная масса, молярный объем, относительная плотность газа.
Примеры решения задач
Пример 1.
1. Назовите по номенклатуре ИЮПАК каждое из следующих соединений:
а)  б)
б) 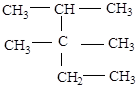
Решение:
а) 2метил3,3диметилпентан;
б) цис-пропилэтилэтилен (цис-гептен-3)
Пример 2.
Охарактеризуйте стадии инициирования, роста и обрыва цепной реакции:
СН3СН2СН3 + Br2 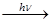 СН3СHBrСН3 +HBr.
СН3СHBrСН3 +HBr.
Решение:
а) инициирование:
Br2 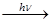 2Br•.
2Br•.
б) рост цепи:
CH3CH2CH3 + Br• ® CH3  HCH3 + HBr.
HCH3 + HBr.
в) обрыв цепи:
CH3  HCH3 + Br•® СН3СHBrСН3.
HCH3 + Br•® СН3СHBrСН3.
Пример 3.
Закончите уравнения следующих реакций и укажите реакции, протекающие по радикальному механизму:
а) С2Н6 + Cl2  ;
;
б) C2H4 + HBr ®;
в) H2C = CH – CH3 + HBr ®;
г) С3Н8 +HNO3 (разб.)  .
.
Назовите продукты реакций.
Решение:
а) C2H6 + Cl2 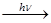 C2H5Cl + HCl;
C2H5Cl + HCl;
механизм радикальный, продукты реакции: C2H5Cl – хлорэтан и HCl – хлороводород.
б) C2H4 + HBr ® С2Н5Br;
продукт реакции: С2Н5Br – бромэтан.
в) H2C = CH - CH3 + HBr ® H3C - CHBr - CH3;
продукт реакции: H3C – CHBr – CH3 – 2-бромпропан.
г) С3Н8 +HNO3 (разб.)  H3C - CH(NO2) - CH3 + H2O;
H3C - CH(NO2) - CH3 + H2O;
механизм радикальный, продукты реакции: H3C – CH(NO2) – CH3 – 2-нитропропан и H2O – вода.
Пример 4.
Напишите схему химических реакций, позволяющих получить из метана хлоропрен:
 .
.
Решение:
CH4  CH3Cl
CH3Cl  C2H6
C2H6 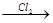 C2H5Cl
C2H5Cl 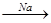 C4H10
C4H10 
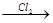


 .
.
Пример 5.
При пропускании 2 л смеси пропана и пропилена через жидкий бром масса склянки с бромом увеличилась на 1,1 г. Определите объемный состав смеси и массу получившихся продуктов.
Дано:
V (смеси) = 2 л
Dm (склянки) = 1,1 г
M (Br2) = 160 г/моль
М (C3H6Br2) = 202 г/моль
Найти:
V (пропана в смеси)
V (пропилена в смеси)
m (продуктов)
Решение:
Найдем количество вещества в смеси, пользуясь следствием из закона Авогадро:
1 моль – 22,4 л
n моль – 2 л
т (смеси) = 0,0892 моль.
С бромом при н. у. взаимодействует только пропилен. Составим уравнение реакции:
С3H6 + Br2 = C3H6Br2.
Пусть в реакцию вступает х г брома, тогда масса образовавшегося дибромпропана равна (1,1 + х). Тогда количество вещества бром равно 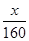 , а количество вещества дибромпропан равно
, а количество вещества дибромпропан равно  . Согласно уравнению реакции 1 моль брома дает 1 моль дибромпропана, следовательно:
. Согласно уравнению реакции 1 моль брома дает 1 моль дибромпропана, следовательно:
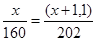 .
.
Решим полученную пропорцию:
202х = 160х + 176, отсюда х = 4,2 г. Тогда количество вещества бром равно:
 (моль).
(моль).
По уравнению реакции n (Br2) = n (C3H6Br2) = n (C3H6) = 0,026 моль.
Отсюда:
m (C3H6Br2) = 202 × 0,026 = 5,30 (г).
m (C3H6) = 42 × 0,026 = 1,09 (г).
n (C3H8) = n (смеси) - n (C3H6) = 0,0892 - 0,026 = 0,0632 (моль).
Отсюда m (C3H8) = 44 × 0,0632 = 2,78 (г).
Найдем объемный состав исходной смеси:

V (C3H6) = 0,026 × 22,4 = 0,58 (л).
V (C3H8) = 0,0632 × 22,4 = 1,42 (л).
Ответ: V (C3H6) = 0,58 л; V (C3H8) = 1,42 л; m (C3H6Br2) = 5,3 г.
Пример 2.
Газ, образовавшийся при полном сгорании 745,7 мл смеси пропана и метана (742 мм рт. ст., 22 °С) может быть поглощен 49,02 мл 5,6 %-ного раствора гидроксида калия (плотность 1,02 г/мл), причем полученный раствор не дает осадка при добавлении к нему раствора хлорида кальция. Определите состав газовой смеси в объемных долях. Рассчитайте объем воздуха (н. у.), который потребуется для полного сжигания указанной газовой смеси.
Дано:
V (смеси) = 745,7 мл
р = 742 мм рт.ст.
t = 22 °С (T = 295 К)
V (р-ра КОН) = 49,02 мл
w (КОН) = 5,6 %
r (р-ра) =1,02 г/мл
Найти:
j (C3H8)
j (CH4)
V (возд.) (н.у.)
Решение:
Приведем объем смеси к нормальным условиям, пользуясь объединенным газовым законом:
 ; тогда
; тогда 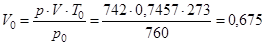 (л).
(л).
Вычислим количества вещества гидроксида калия, вступившего в реакцию:
m (р-ра КОН) = r × V = 1,02 × 49,02 = 50 (г).
 (г);
(г);
 (моль).
(моль).
При сгорании смеси пропана и метана образуется углекислый газ. Вычислим его объем.
Запишем уравнение реакции взаимодействия углекислого газа с гидроксидом калия:
CO2 + KOH = KHCO3.
Поскольку полученный раствор не дает осадка при добавлении раствора хлорида кальция, реакция между углекислым газом и гидроксидом калия прошла до конца.
По уравнению реакции n (KOH) = n (CO2) = 0,05 моль.
Отсюда V (CO2) = n × Vm = 0,05 × 22,4 = 1,12 (л)
Запишем уравнения реакции горения смеси.
СН4 + 2О2 = СО2 + 2Н2О. (1)
С3Н8 + 5О2 = 3СО2 + 4Н2О. (2)
Составим пропорции, по этим уравнениям обозначив объем метана за х и объем выделившегося углекислого газа при горении метана за y. Тогда объем пропана (0,675 - х), а объем выделившегося углекислого газа при горении пропана (1,12 - y).
По уравнению (1)  .
.
По уравнению (2)  .
.
Решим систему из этих двух уравнений:
 ,
,
x = 0,452 (л). Следовательно, V (CH4) = 0,452 л.
Тогда V (C3H8) = V (смеси) - V (CH4) = 0,675 - 0,452 = 0,223 (л).
Зная объем смеси и объемы её компонентов, найдем объемные доли метана и пропана.
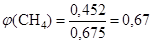 ;
;
 .
.
Для нахождения объема воздуха, необходимого для полного сжигания смеси, определим количество вещества метана и пропана.
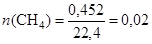 (моль);
(моль);
 (моль).
(моль).
По уравнению реакции (1) на 1 моль метана расходуется 2 моля кислорода. Следовательно, количество вещества кислорода составляет 2 × 0,02 = 0,04 моль.
По уравнению реакции (2) на 1 моль пропана расходуется 5 молей кислорода. Следовательно, количество вещества кислорода составляет 5 × 0,01 моль = 0,05 моль.
Общий объем кислорода пошедший на горение смеси пропана и метана равен:
V (O2) = (0,05 моль + 0,04 моль) × 22,4 = 2,01 (л).
Так как в воздухе кислорода находится 21 % (об.), то
 (л).
(л).
Ответ: j (СН4) = 0,67; j (С3Н8) = 0,33; V (O2) = 9,57 л (н. у.).
|
из
5.00
|
Обсуждение в статье: ЗАДАНИЯ ДЛЯ УЧАЩИХСЯ 10 КЛАССА |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

