 |
Главная |
III. Реакции по радикалу
|
из
5.00
|
1) Замещение на галоген в алифатических альдегидах или кетонах.
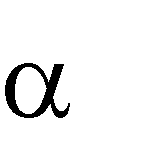 Наличие в молекуле альдегидов электроноакцепторной карбонильной группы приводит к повышению полярности связи С-Н у соседнего углеродного атома ( -положении по отношению к карбонилу). Это приводит к облегчению разры- ва связи, повышению реакционной способности атомов – их легкому замеще- нию, например на галоген. В альдегидах на свету:
Наличие в молекуле альдегидов электроноакцепторной карбонильной группы приводит к повышению полярности связи С-Н у соседнего углеродного атома ( -положении по отношению к карбонилу). Это приводит к облегчению разры- ва связи, повышению реакционной способности атомов – их легкому замеще- нию, например на галоген. В альдегидах на свету:
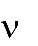
| h |
 O O
O O
CH3 C Cl2 CH2 C
H -HCl
Cl H
Для кетонов в щелочной среде при действии галогенов (I2, Cl2) образуют- ся йодоформ или хлороформ. Реакция образования йодоформа используется в клинике для обнаружения ацетона в моче:
CH3 C CH3 + 3 J2 CJ3 C CH3
O -3HJ O
Йодоформ легко разлагается при нагревании. Эти превращения являются каче- ственной реакцией на кетоны с метильной группой.
CH3 C
t
| CJ3 + H |
CHJ3
O
+ CH3 C
O Йодоформ
(желтый)
характерный запах
ONa
Ацетат натрия
2) Реакции, характерные для ароматических радикалов – электро- фильное замещение (SЕ).
Карбонильная группа, являясь акцептором электронов понижает элек- тронную плотность в бензольном кольце, но меньше всего в мета-положении к карбонилу. То есть является ориентантом II-рода – затрудняет протекание элек- трофильного замещения и направляет атаки в положение 3,5-
O
C
H
+Br2
t0 FeBr3
| O |
| C |
| H |
Br
3-бромбензальдегид
3) Реакции, характерные для непредельных альдегидов:







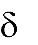
 ' O + -
' O + -
CH2 CH C
+ HBr
CH2 CH2
CHO
' H Br
Акролеин 3-Бромпропаналь
Присоединение галогенводородов происходит против правила Марковни- кова. Это определяется тем, что акцепторная карбонильная группа проявляет
отрицательный индуктивный, а в α,β-непредельных кетонах и отрицательный мезомерный эффект. Смещение электронной плотности π-связи происходит в сторону карбонильной группы и возникновению частично-положительного и отрицательного заряда, что и определяет направление присоединения.
IV. Реакции восстановления и окисления.
Реакции окисления
Альдегиды легко окисляются в соответствующие карбоновые кислоты. Для их окисления можно использовать сильные окислители, такие как KMnO4, и сла- бые, такие как аммиачный раствор оксида серебра (Ag2O, проба Толленса) и гидроксид меди (II) (Cu(OH)2, проба Троммера).
Проба Толленса (реакция серебряного зеркала):
H3C - C
O
+ 2[Ag(NH3)2]OH
H
toC
2 Ag + 4NH3 + H2O +
O
H3C - C
OH
В результате реакции на стенках пробирки образуется серебро в мелко- дисперсном состоянии, образуя зеркало. Эта реакция используется как каче- ственная реакция на альдегидную группу.
Проба Троммера (реакция медного зеркала):
H3C - C
O + Cu(OH) toC Cu O + H O + H C - C
| 2 32 2 |
| O |
В результате реакции, при нагревании образуется оранжевый налет ок- сида меди (I) на стенках пробирки, поэтому эта реакция используется как ка- чественная реакция на альдегидную группу.
Кетоны окисляются с трудом, только сильными окислителями. При этом образуется смесь карбоновых кислот.

| 3 |
H3C
CH2 C
CH3 CH
CH2
COOH,
O 2) 2CH3COOH
|
из
5.00
|
Обсуждение в статье: III. Реакции по радикалу |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

