 |
Главная |
Одноосновные карбоновые кислоты
|
из
5.00
|
Электронное строение карбоксильной группы
Карбоксильная группа является сочетанием двух функциональных групп карбонильной и карбоксильной:




| C O |




| C O H |
| O |



| + |
' '+
M VEUAAAAAAAClZ7nPAAAAAXRSTlMAQObYZgAAAAlwSFlzAAAh1QAAIdUBBJy0nQAAAChJREFUSEvt yiEOADAMA7Hs/58eCZoKRyrZ9C4AsMaZtc76vFoB/kou20YAL3VTh0sAAAAASUVORK5CYIJQSwEC LQAUAAYACAAAACEAsYJntgoBAAATAgAAEwAAAAAAAAAAAAAAAAAAAAAAW0NvbnRlbnRfVHlwZXNd LnhtbFBLAQItABQABgAIAAAAIQA4/SH/1gAAAJQBAAALAAAAAAAAAAAAAAAAADsBAABfcmVscy8u cmVsc1BLAQItABQABgAIAAAAIQDeEdlABwcAAJAhAAAOAAAAAAAAAAAAAAAAADoCAABkcnMvZTJv RG9jLnhtbFBLAQItABQABgAIAAAAIQAubPAAxQAAAKUBAAAZAAAAAAAAAAAAAAAAAG0JAABkcnMv X3JlbHMvZTJvRG9jLnhtbC5yZWxzUEsBAi0AFAAGAAgAAAAhAODkqXfhAAAACgEAAA8AAAAAAAAA AAAAAAAAaQoAAGRycy9kb3ducmV2LnhtbFBLAQItAAoAAAAAAAAAIQBvi9MYWgIAAFoCAAAUAAAA AAAAAAAAAAAAAHcLAABkcnMvbWVkaWEvaW1hZ2UxLnBuZ1BLAQItAAoAAAAAAAAAIQA66C/WsgAA ALIAAAAUAAAAAAAAAAAAAAAAAAMOAABkcnMvbWVkaWEvaW1hZ2UyLnBuZ1BLBQYAAAAABwAHAL4B AADnDgAAAAA= "> 

 H
H
- I, +M
Негибридная р-орбиталь кислорода гидроксильной группы вступает в сопряжение с π-связью карбонильной группы.







| . O |
| . C |
| .. O |
В сопряженной системе электронная плотность выровнена, частично по- ложительный заряд на атоме углерода невелик, поэтому для кислот не харак-
терны реакции нуклеофильного присоединения по карбонильной группе. Вследствие сопряжения кислород, испытывающий недостаток электронов, притягивает электроны связи О-Н сильнее. Полярность связи О-Н повышается, что повышает кислотность карбоновых кислот по сравнению со спиртами. Со- пряжение обеспечивает стабильность карбоксилат-иона, что так же повышает кислотность:


| O |

 R C R C
R C R C
OH
O-1/2
+ H+
O -1/2
На изменение реакционной способности кислот влияет характер радикала (R). Электроноакцепторные заместители увеличивают кислотность, донорные- понижают. Поэтому самой сильной кислотой гомологического ряда предельных одноатомных кислот является муравьиная, ароматические кислоты сильнее алифатических (за счет увеличения цепи сопряжения), многоосновные кислоты сильнее одноосновных.
Химические свойства
Для карбоновых кислот характерны реакции замещения атома водорода в гидроксильной группе (кислотность), реакции замещения гидроксильной груп-
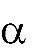
| - |
ложении), т.к. группа карбоксильная группа проявляет отрицательный индук- тивный эффект и увеличивает подвижность атомов водорода в радикале.




| O C |
| + |
| O |
| ' |
| H |



| замещение H |
| H |
| R |
| CH |




CH-кислотный центр
Электро- фильный центр
кислотность
 образование солей
образование солей
 '+
'+

Кислотный центр
1. Кислотно-оснóвные свойства.
| H |
RCOOH
RCOO - + +
Кислоты образуют соли с активными металлами, основными оксидами, осно- ваниями и солями более слабых кислот:
CH3
2 Na
O Na2O
C +
NaOH
O H
CH3
O
C

O Na
H2
H2O
+
H2O
уксусная кислота
Na2CO3
ацетат натрия
H2O + CO2
Карбоновые кислоты относятся к слабым электролитам, поэтому их соли в растворе частично гидролизованы, а под действием сильных кислот разлага- ются:
CH3
O
C
O Na
+ HCl
O
CH3 C
O
+ NaCl
H
ацетат натрия
уксусная кислота
2. Реакции нуклеофильного замещения (SN) гидроксильной группы (обра- зования функциональных производных).
Это наиболее важные, легко протекающие реакции, приводящие к об- разованию различных функциональных производных карбоновых кислот - галогенангидридов, ангидридов, амидов, сложных эфиров.
1) Образование сложных эфиров (реакция этерификации).
CH3
O


| 2 4 |
t0, H SO
CH3
C + H2O
| O |
уксусная кислота метиловый
спирт
метиловый эфир
уксусной кислоты (метилацетат)
2) Образование галогенангидридов происходит в реакции карбоновых ки- слот с пентахлоридом фосфора или хлористим тионилом.
CH3 C
O

 + PCl5
+ PCl5
to
CH3 C
O

 + POCl3 + HCl
+ POCl3 + HCl
OH Cl
хлорангидрид уксусной кислоты




| 2 |
CH3 C
+ SOCl to OH
CH3 C
+ SO2 + HCl
Cl
3) Образование амидов.

 O
O
CH3 C
+ NH3
O to
CH3 C
O
CH3 C
+ H2O
OH O
ацетат аммония

NH4
амид
NH2
CH3
O

 C + NH2 OH
C + NH2 OH
O
to
R CH3 C
HN
уксусной кислоты
+ H2O
R
алкиламид уксусной кислоты
|
из
5.00
|
Обсуждение в статье: Одноосновные карбоновые кислоты |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

